유연 디스플레이 커버 윈도우용 초박형 유리의 화학강화
Chemical Strengthening of Ultra-Thin Glass for Use as Cover Window of Flexible Displays
Article information
Trans Abstract
The recent commercial success of foldable smartphones is indebted in part to integration of ultra-thin glass (UTG) into the flexible display modules. To endow glass with such a foldability, while keeping its merits over polymeric materials, tons of complicated issues need to be resolved in addition to thickness reduction. Since UTG is subjected to repeated deformations during its service as a flexible cover window, extra care is required to minimize microcracks during the whole preparation process. Here, it is noteworthy that chemical strengthening via ion exchange should be performed to UTG for better durability. In this article, after briefly reviewing the current status of UTG in terms of production and process, its chemical strengthening is highlighted as a viable option to further innovate its functionalities. A new ion-exchange technique which is not adopting the molten-salt-bath is proposed, and some experimental demonstrations exemplifying the concept of ‘actively stress-managed glass’ are delineated.
1. 서론
스마트폰을 위시한 모바일 전자기기는 일상 생활의 필수재가 되었으며 거의 대부분 정보의 입출력이 디스플레이 모듈을 통하여 이루어진다. 해당 모바일 디스플레이의 커버 윈도우는 공통적으로 유리소재를 채용하고 있음은 주지의 사실이다. 기존 리지드 폼 팩터(rigid form-factor) 디스플레이의 커버 윈도우용 유리는 기계적 안정성을 갖추고 있으며 동시에 고유의 사용자 경험을 제공하고 있다. 한편, 폴더블(foldable) 스마트폰과 같은 유연 디스플레이 모듈을 채용하는 전자기기는 향후 슬라이더블(slidable), 롤러블(rollable) 등의 폼 팩터를 거쳐 궁극적으로 스트레처블(stretchable) 형태로 다변화될 것으로 판단된다. 폴더블 스마트폰의 성공적인 시장진입은 일정 부분 초박형 유리(UTG; ultra-thin glass)의 양산 및 실제 적용에 힘입은 것으로 알려져 있다. 디스플레이 모듈에 특정 형태의 형상 가변성을 부여하기 위해서는 해당 디스플레이 모듈의 전체 구성요소에 특정 변형동작이 반복적으로 가능할 수 있도록 유연성을 부여하여야 한다. 즉, OLED 패널과 더불어 접합소재 및 커버 윈도우 소재 각각의 두께와 탄성계수를 최적화하여 접합 후 각 구성요소 및 계면에서 발생하는 응력을 최소화함과 동시에 디스플레이 모듈 본연의 기능을 수행할 수 있도록 해야 한다. 이를 고려하면, 유연 디스플레이 모듈의 구현에 있어 커버 윈도우 소재는 디스플레이 패널을 열적/기계적/화학적 측면에서 보호하면서도 기존 리지드 디스플레이 모듈의 화학강화 유리 기반 커버 윈도우에 대한 고유의 심미성 및 터치감을 가급적 유지할 필요가 있으므로 관련 기술적 난이도가 높다고 볼 수 있다.
출시 초기의 폴더블 스마트폰은 변형 동작 내구성을 확보하기 위하여 고분자 계열 소재 중에서 탄성계수가 비교적 높은 폴리이미드 소재에 가시광 대역의 투과도를 부여한 투명 폴리이미드(CPI; colorless polyimide)를 적용하였다.[1] 그러나 CPI 소재는 유리 소재와 비교하여 경도와 탄성계수가 작기 때문에 표면 긁힘에 취약하고 주름이 쉽게 발생할 수 있다. 이러한 현상의 발생빈도를 낮추기 위하여 최근에는 경도와 탄성계수가 현저히 높은 유리 소재를 커버 윈도우로 적용한 폴더블 스마트폰이 출시되어 높은 시장점유율을 확보하고 있다.[2] 구체적으로 설명하면, 유리 소재의 탄성계수가 태생적으로 고분자 소재보다 현저히 크기 때문에 유연성을 부가하기 위해서는 기존 리지드 스마트폰용 커버 윈도우 유리 대비 1/10 이하 수준으로 두께가 얇아진 초박형 유리를 폴더블 스마트폰에 적용하고 있으며, 향후 UTG는 대면적 폴더블 노트북 PC와 더불어 슬라이더블 또는 롤러블 디스플레이에도 적용될 수 있을 것이다.
유리 소재의 경우 강도, 경도 및 변형동작 내구성 등의 물성을 추가적으로 향상시키기 위하여 강화공정을 통하여 표면부에 압축응력을 부가할 수 있는데, 이러한 공정은 유리 소재 고유의 열적/기계적 성질을 활용하여 이루어지기 때문에 일반적인 고분자 소재에는 적용성이 낮다. 따라서 물리강화(physical strengthening) 및 화학강화(chemical strengthening) 공정은 유리 본연의 기계적 물성을 구현하는데 있어 매우 중요하며, 여타 소재와 차별되는 유리 소재의 특성으로 간주할 수 있다. 전술한 바와 같이, UTG는 얇은 두께를 전제로 하기 때문에 열처리 공정을 통한 물리강화의 효과가 없어서 이온교환(IX; ion exchange) 공정을 통한 화학강화를 거쳐 표면부에 압축응력을 부여한다.[3,4] 따라서 화학강화를 통하여 UTG의 기계적 물성을 향상시킬 수 있으며, 이를 위한 이온교환 공정은 전체 UTG 제작 공정의 수율을 좌우하는 중요한 공정이다. 유리는 대표적인 취성 재료(brittle material)이며, 제조공정 또는 사용 중에 표면에서 발생하는 미세균열이 초래하는 응력집중(stress concentration) 현상에 기인하여 실제 강도(practical strength)가 이론 강도(theoretical strength)보다 현저히 낮아진다. 따라서 표면에 존재하는 미세균열이 압축응력이 인가된 영역 내에 위치하면 해당 미세균열에 가해지는 응력집중을 낮추어 실제 강도를 향상시키게 된다. Fig. 1에 도시한 바와 같이, 일반적으로 화학강화는 유리 내부에 존재하는 소듐 이온을 상호확산(interdiffusion)을 통하여 반지름이 더 큰 포타슘 이온으로 치환하는 경우에 발생하는 충진 효과(stuffing effect)에 의한 압축응력을 활용하며, 이미 1960년대부터 그 현상이 보고되었음에도 실제 적용분야는 제한적이었으나 스마트폰의 출현과 더불어 대규모 산업적 적용이 이루어졌다.[4] 화학강화 공정은 크게 습식(침지 방식) 공정과 건식(비침지 방식) 공정으로 대별된다. 습식 공정의 경우, 용융상태로 존재하는 KNO3 등의 알칼리염에 유리를 침지하여 이온교환을 달성하는 반면에 건식 공정의 경우에는 용융상태의 알칼리 염욕(salt bath)을 사용하지 않고 알칼리 이온을 함유하는 슬러리를 유리 표면에 분사하거나 도포하고 이를 열처리하여 이온교환을 달성한다.
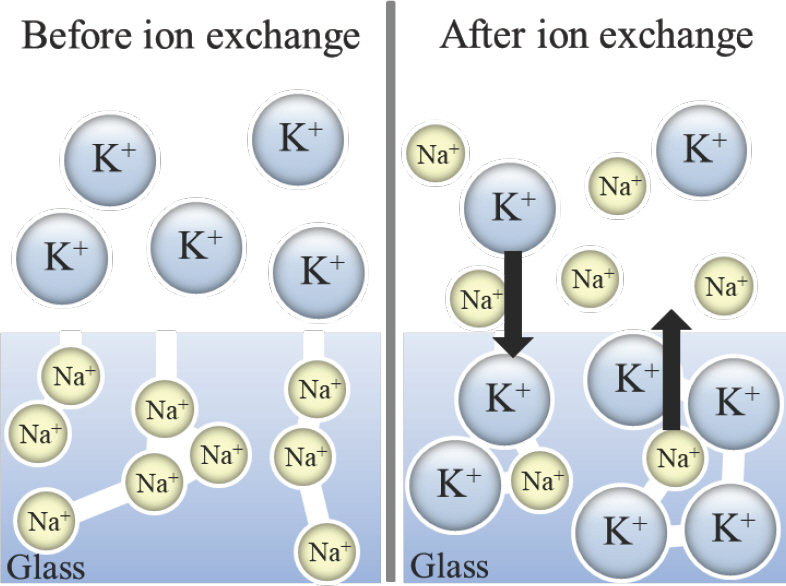
Illustration showing spatial distributions of Na+ and K+ ions before and after ion exchange process for chemical strengthening of sodium-containing silicate glass.
본 논문에서는 유연 디스플레이 모듈에 적용되고 있는 UTG의 조성, 물성 및 제조공정을 개략적으로 소개하고 UTG 대상 화학강화의 기본원리와 공정을 설명한다. 특히, UTG를 대상으로 수행되는 이온교환을 통한 화학강화의 기여도를 UTG의 유연성 개선 효과를 중심으로 기술하였으며, 새로운 건식 이온교환 공정에 기초하여 유리에 추가적인 기능성을 부여하는 개념과 연관된 실험 사례를 집중적으로 소개하고자 한다.
2. 유연 디스플레이용 커버 윈도우 소재의 변형 관련 요구조건
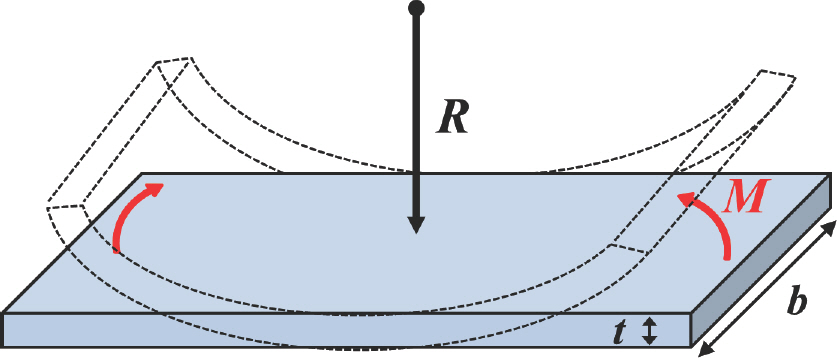
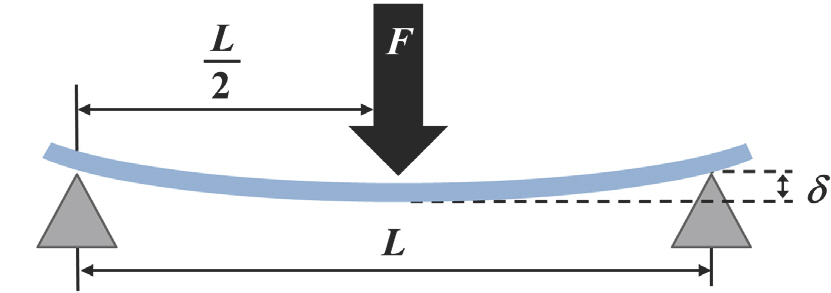
유연 디스플레이용 커버 윈도우 소재의 유연성은 굽힘 변형에 대하여 해당 소재가 버티는 정도를 나타내는 굽힘 강성(K; bending stiffness)에 의해 결정된다. 균일한 조성과 두께를 가지는 판재가 외부에서 가해지는 하중에 의하여 탄성적으로 휘어지는 상황을 Fig. 2에 도시하였다. 이러한 상황에서 해당 판재의 K는 굽힘 모멘트(M; bending moment), 곡률 반경(R; radius of curvature) 및 판재의 너비(b)를 포함하여
여기에서 M은 탄성계수(E; elastic modulus)와 관성 모멘트(I; moment of inertia) 및 R에 대하여
일반적으로 고분자 소재는 미세구조의 특성상 유리 소재보다 뚜렷하게 낮은 탄성계수를 가진다. 실제로 CPI 소재의 탄성계수는 ~6 GPa 수준으로 UTG 소재의 탄성계수인 ~70 GPa 대비 매우 낮은 값을 가진다.[6] 이는 두 소재의 두께가 동일하다면 유사한 곡률 반경을 얻기 위해서는 UTG에 10배 이상의 힘이 작용하여야 함을 의미하며, UTG에 미세균열이 존재할 때 발생하는 응력집중 현상이 커져서 파단이 초래될 가능성이 커지게 된다. 따라서 UTG 소재의 경우 미세균열을 더욱 세심하게 관리하여야 하며, 나아가 이온교환 공정을 통하여 경도 및 강도를 향상시키는 화학강화의 효과가 상대적으로 더욱 중요하게 된다. 한편, 경도와 내마모성 등의 표면 물성은 탄성계수에 비례하는 경향을 보이기 때문에 CPI 소재의 상대적으로 낮은 탄성계수는 유연 디스플레이의 커버 윈도우로서 표면 품질의 저하를 초래하며, 반복적으로 응력이 집중되는 부분에서 주름 등과 같은 비가역적인 변형을 발생시킬 가능성이 크다.[2] 따라서 CPI 소재의 경우에는 불필요한 변형을 최소화하는 방향으로 탄성계수 및 두께를 제어할 필요가 있으며, UTG 소재의 경우에는 두께 제어와 더불어 미세균열 최소화와 화학강화를 통한 기계적 물성의 향상이 중요하다.
3. 초박형 유리의 조성 및 제조공정
실리케이트 유리(silicate glass)는 주요 구성성분이 지구 표면에 방대하게 존재하는 원소들이어서 환경친화적이고 제조비용이 상대적으로 저렴하다.[7] 실리케이트 유리 특유의 구조적 안정성과 조성의 다양성은 SiO 결합의 고유한 화학결합 특성에 기인한다. 즉, 실리케이트 유리에서 실리콘 원자와 산소 원자는 ~50% 수준의 공유결합성을 가지는데, 이에 기인하여 실리콘 원자는 [SiO4] 사면체 단위구조를 형성하며 구조적으로 안정한 3차원 망목 구조를 만들게 된다. 한편, SiO 결합을 이온결합성 측면에서 보면 Si4+ 이온과 O2- 이온 사이에서 요구되는 전기적 중성도 조건을 만족하기 위하여 [SiO4] 사면체에는 SiO-Si 결합에 참여하는 가교 산소(bridging oxygen)와 더불어 추가적인 전하보상이 필요한 SiO1- 형태의 비가교 산소(nonbridging oxygen)가 혼재하여 매우 다양한 1+ 또는 2+ 전하를 띄는 양이온을 구성 성분으로 포함하여 유리를 형성할 수 있다.[8] 가장 대표적인 실리케이트 유리는 소다라임 실리케이트(SLS; soda-lime silicate) 계열 조성의 유리이며, 이온교환을 통한 화학강화가 가능하다. 한편, 디스플레이용 커버 윈도우로 적용되는 실리케이트 유리는 대부분 소듐-알루미노실리케이트(SAS; sodium-aluminosilicate) 유리이며, Na+ 이온이 [AlO4]1- 사면체의 전하보상제 역할을 하도록 조성비를 제어함으로써, 전형적인 망목수식제로 작용하는 경우와 대비하여, Na+ ↔ K+ 이온교환 과정의 확산계수를 크게 하여 화학강화 효과가 SLS 유리보다 뛰어나다.
UTG는 일반적으로 100 μm 이하의 두께를 가지기 때문에 태생적으로 이온교환공정에서 확산 깊이(DOL; depth of layer)를 용이하게 제어할 수 있는 자유도가 높지 않아서 비교적 단순하고 전통적인 SAS 조성을 가진다. 두께가 100 μm 수준인 SLS 조성의 UTG가 전형적인 플로트 공법으로 제조될 수 있으나, 아직까지 표면 평탄도 및 소위 air-side와 tin-side의 광학적/화학적 이방성과 연관된 문제점을 가진다. Fig. 4에 도시한 것처럼 디스플레이용 커버 윈도우 적용을 위한 UTG는 오버플로우(overflow) 공법과 다운드로우(down-draw) 공법을 통하여 제조된다.[9,10] 오버플로우 공법은 적절하게 점도가 제어된 융체를 백금 구조물로부터 흘러 넘치도록 하여 UTG를 만들며, 점도와 자중이 균형을 이루어 두께가 결정된다. 다운드로우 공법의 경우, 융체를 백금으로 제작된 슬릿에 통과시키고 롤러를 이용함으로써 보다 능동적으로 두께를 제어할 수 있다. 오버플로우 공법에서는 표면 평탄도가 매우 우수한 UTG를 만들 수 있는 반면에 두께를 작게 유지하는 것이 어려운 것으로 알려져 있다. 이와 달리 다운드로우 공법의 경우 두께를 작게 하는 것이 용이한 반면에 유리 표면과 롤러와의 접촉에 기인하는 표면 평탄도의 저하가 발생할 수 있다. 한편, 화학적 식각(슬리밍; slimming) 공정을 통하여 수백 μm 두께의 유리를 수십 μm 수준의 UTG로 만드는 공정도 활발하게 적용되고 있다.
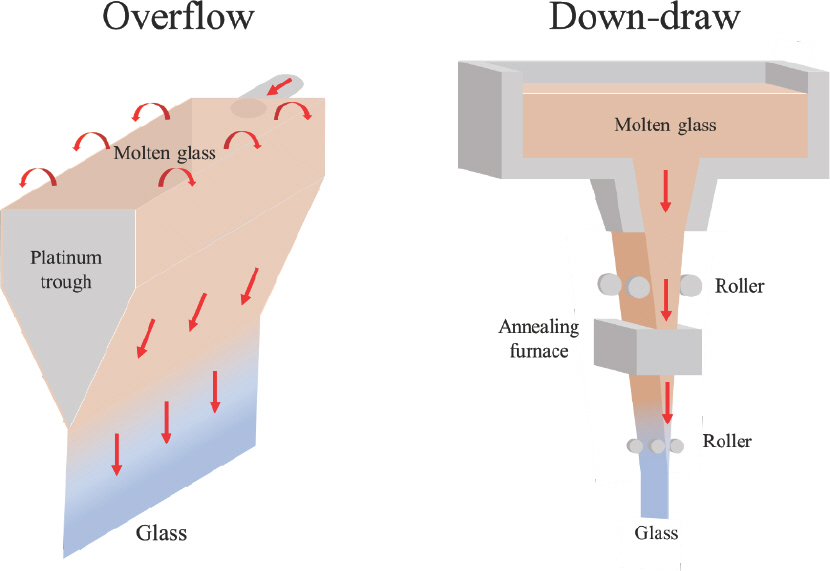
Schematic drawings for the overflow process (left) and the down-draw process (right) for forming pristine UTG.
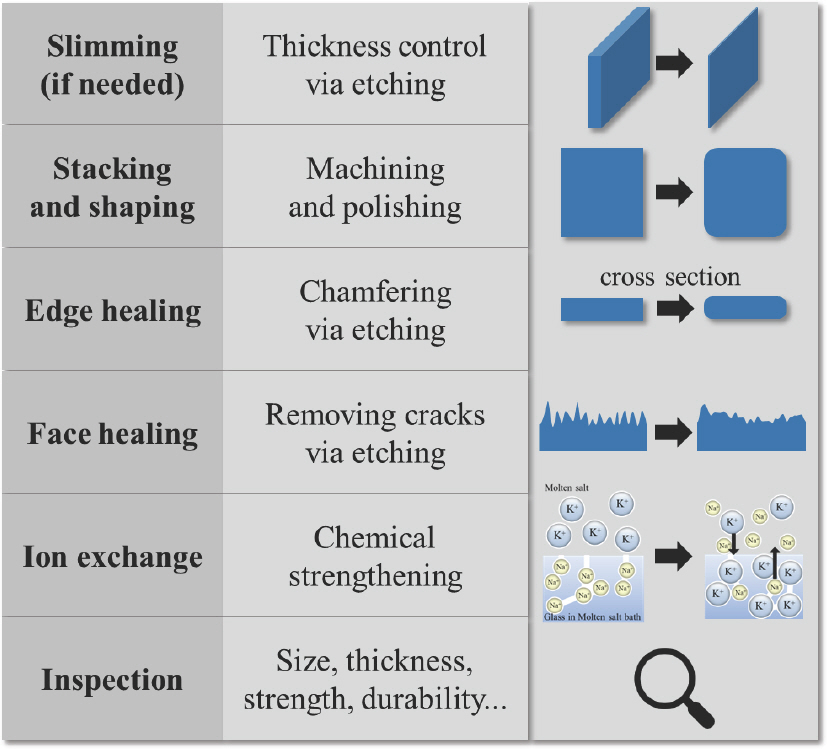
상기 공법을 통하여 제작된 UTG를 유연 디스플레이용 커버 윈도우로 적용하기위해서는 Fig. 5에서 확인할 수 있듯이 다양한 후속 공정이 필요하다. 일반적이며 대표적인 공정을 설명하면, 우선 적절한 두께를 가지는 UTG를 적층한 뒤 기계적인 방법으로 절단하고 연마한 후에 식각을 통해 모서리를 둥글게 가공하는 챔퍼링(chamfering) 단계를 거친 후 UTG 셀의 표면에 발생한 평탄도 저하를 식각을 통하여 완화시킨다. 이후 표면처리가 완료된 UTG에 이온교환 공정을 적용하여 화학강화 효과를 부여하게 된다. 각 단계에서 불필요한 형상의 변화 및 미세균열의 발생을 최소화하는 것이 매우 중요하며, 공정 비용의 추가적인 절감 및 수율 향상을 위한 다양한 연구개발이 필요하다. 아직까지도 유연 디스플레이 모듈의 커버 윈도우용 UTG와 관련된 기술적 장벽이 다수 존재하며, 잠재적으로 파급효과가 큰 돌파구는 3개로 요약될 수 있다. 첫째로, UTG의 조성 제어를 통하여 보다 유연하면서도 화학강화 효과가 큰 유리 조성을 탐색하는 것이다. 일례로, UTG의 변형특성에 가장 큰 영향을 미치는 인자인 탄성계수는 Makishima-Mackenzie 모델을 적용하여 구성 원자 사이의 해리에너지와 각 원자의 충진율 및 조성비를 활용하여 정량적으로 유추할 수 있으며,[11] 최근에는 기계학습 등의 방법론도 활발히 적용되어 기존 SAS 조성의 UTG보다 낮은 탄성계수를 가지는 조성을 탐색할 수 있다. 그러나 낮은 탄성계수는 표면경도 등의 기계적 물성을 저하시키며 화학강화 효과 역시 저하시키는 부수적인 효과를 야기하기 때문에 UTG의 요구조건을 모두 만족하는 새로운 조성을 찾는 것이 매우 어렵고, 이와 동시에 해당 조성을 초박형으로 두께를 낮추는 공정을 확보하는 것 역시 난이도가 높다. 둘째로, UTG 공정에 투입되는 비용의 절감을 위하여 각 공정 단계를 최적화하는 것이다. 일례로, UTG 원장별로 레이저 가공을 통하여 면취하고,[12] 광학적 또는 화학적 방법으로 챔퍼링하여 적층 및 연마 단계를 없애는 공정을 적용할 수 있을 것이다. 마지막으로, 유리 소재에만 적용될 수 있는 이온교환 공정을 보다 적극적으로 활용하는 것이다. 기존 이온교환은 공히 용융상태의 염욕에 유리를 침지하는 방식을 활용하는데, 이러한 습식(또는 침지 방식) 공정은 해당 유리의 모든 면에 균일한 압축강도와 확산 깊이를 제공하게 된다. 이와 반면에 건식(또는 비침지 방식) 공정에 기반한 이온교환 기술을 확보하는 경우, 유리 표면의 임의의 위치에 임의의 형상으로 이온교환을 발생시킬 수 있게 된다. 이와 같이 위치 선택적 이온교환 기술을 활용하여 소위 능동 응력제어 유리(ASMG; actively stress managed glass)를 구현할 수 있다. 즉, ASMG를 통하여 유리 형상을 그대로 유지하면서 표면 응력의 크기와 공간적 분포를 제어하거나, 변형동작에 적합하도록 의도적으로 소성변형을 인가하여 동작 특성을 최적화하는 등의 추가적인 기능성을 부여할 수 있다. 이와 관련된 세부적인 구현 사례는 아래에서 예시적으로 기술하였다.
4. 초박형 유리의 강화
유리 소재의 취성은 구성 원자 사이의 공유결합 및 이온결합 특성과 원자 배열특성에 기인한다. 전술한 바와 같이, 실리케이트 유리에서 형성되는 SiO 결합의 공유결합성으로 인하여 [SiO4] 사면체는 이웃한 사면체와 특정한 방향성을 가지면서 연결되기 때문에 해당 망목의 충진도는 전형적인 금속결합성 고체와 비교하여 현저히 낮아진다.[13] 이와 더불어, 이온결합성으로 인한 전기적 중성도 유지가 필요하므로 금속 소재에서 쉽게 관찰되는 전위와 같은 1차원 결함의 형성이 매우 어렵다. 또한, 실리케이트 유리 소재는 태생적으로 중거리 이상의 규칙도가 존재하지 않기 때문에 전위의 이동을 원활하게 하는 슬립 시스템(slip system)이 부재하여 외부에서 힘이 작용하는 경우 소성변형을 일으키지 못하고 바로 파단에 이르게 된다. 유리와 같은 취성 재료가 나타내는 이론 강도 대비 현저히 낮은 실제 강도(σ m)는 Griffith-Inglis 이론에 의해 미세균열의 길이(2a)와 매우 밀접한 연관을 가지며,
유리 소재 고유의 취성에 대한 이해를 바탕으로 파단을 줄이기 위한 연구가 다양한 측면에서 진행되어 왔는데,[4,18] 이러한 방법론은 크게 3개로 분류될 수 있다. 첫 째, 유리의 미세구조 최적화를 통하여 파괴인성(K IC)을 높이는 것이다. 유리 내부에 결정상을 분포시켜서 균열의 전파를 저해하는 방식은 잘 알려진 결정화 유리(glass-ceramics)의 인성 및 내충격성 향상 기구이며, 석출 결정상의 굴절률과 입도를 제어하여 투명도를 유지하면서도 기계적 물성의 향상을 도모할 수 있으며, 향후 초박형 결정화 유리에 대한 개발이 필요하다. 둘째, 표면결함 자체를 감소시켜 응력집중계수(K I; stress concentration factor)를 낮추는 것이다. 유리와 같은 열가소성 물질의 표면부를 화염이나 레이저 등의 가열원에 노출시켜서 미세균열을 제거하는 가열 연마(fire polishing) 공정이 대표적이며, 화학적 식각 공정도 효과적이다. 또한, 유리 표면에 보호 또는 강화 기능의 코팅을 부가하여 응력집중을 낮출 수 있다. 셋째, 유리 표면에 압축응력을 인가하여 실제 강도를 증진시키는 방법이며, 표면에 존재하는 미세균열의 첨단부가 압축응력 영역 안에 위치하면 부가된 압축응력만큼 응력집중이 감소하여 실제 강도가 향상된다. 유리의 제조 및 후속 가공공정에서 미세균열의 도입을 완벽하게 제거하는 것이 매우 어렵기 때문에 일반적으로 기계적 물성을 제고하기 위하여 표면부에 압축응력을 부여하는 강화 공정을 거치며, 주로 물리강화 및 화학강화 방식이 적용된다.
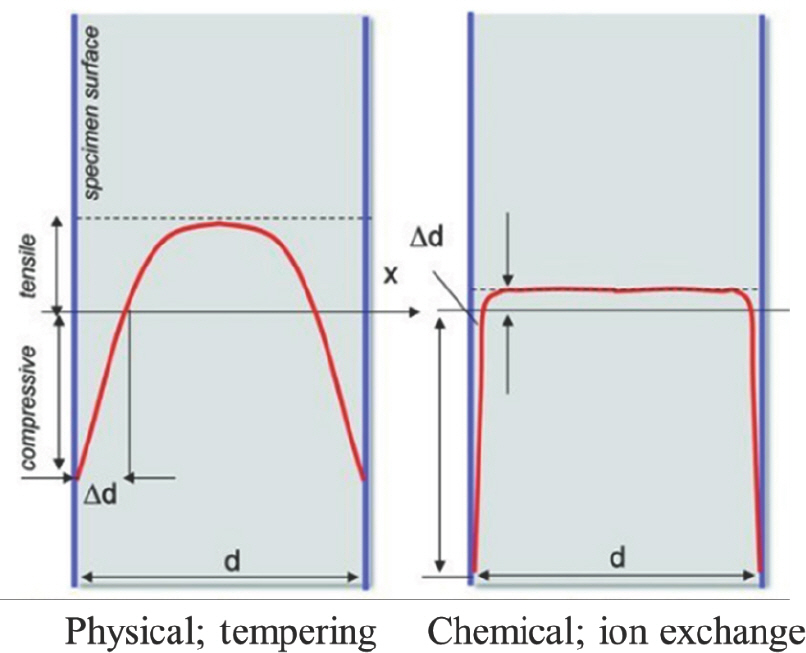
물리강화는 유리를 유리전이온도 이상으로 가열한 후 표면에 압축공기를 불어서 표면과 내부의 냉각속도 차이를 유발시키는 방식이며 열강화라고도 지칭된다. 상대적으로 빠르게 냉각되는 표면부가 내부에 비하여 보다 큰 몰 부피(molar volume)을 가지려는 경향을 보이므로 상온으로 냉각된 상태에서 표면부에는 압축응력이 인가되고 내부에는 인장응력이 인가된다. 물리강화를 거친 유리의 위치별 응력분포는 냉각과정에서 형성되는 온도분포에 의하여 영향을 받기 때문에 일반적으로 포물선 형태의 응력분포를 나타내며, 이러한 분포는 이온교환에 의하여 야기되는 포타슘 이온의 농도분포에 의존하여 압축응력을 발생시키는 화학강화의 응력분포와 대별된다. Fig. 7에 도시한 바와 같이, 화학강화에서는 표면부의 최대 압축응력이 상대적으로 크고 중앙부의 인장응력 영역이 낮고 길게 형성되는 태생적 차이를 보인다.[19] 물리강화 방식의 경우 유리의 내부와 외부의 냉각속도 차이가 클수록 효과적이기 때문에 복잡한 형상을 가지는 유리 또는 두께가 얇은 유리로의 적용성이 낮아진다. 일반적으로 3 mm 이하의 두께를 가지면 물리강화 효과가 뚜렷하지 않은 것으로 인식된다.[20] 최근 들어 탄소중립화 및 플라스틱 소재의 환경오염 등의 이슈가 대두되면서 유리 분야에서도 판유리의 박형화 및 병유리의 경량화 관련 연구개발이 진행되고 있다. 이러한 추세는 공통적으로 물리강화 방식보다는 화학강화 방식의 효용성을 부각시킴을 알 수 있다.
이미 앞에서 기술한 바와 같이, 이온교환을 통한 화학강화는 1960년대부터 알려졌으며,[21] 기초적인 이온교환 거동 및 강화 특성 등의 연구가 진행되었으나 산업적 응용분야는 크게 활성화되지 않았다. 즉, 항공기의 조종석 캐노피 등의 특정 수요분야에서 적용되었으며, 급성 알레르기 반응과 같은 응급상황에 필요한 액상 약제를 담지하는 소듐-보로실리케이트(sodium-borosilicate) 유리의 기계적 안정성을 화학강화 방식을 통하여 현저히 높인 사례는 잘 알려져 있다. 그러나 2007년에 출현한 스마트폰의 커버 윈도우로서 SAS 유리가 적용되고 이를 이온교환 방식으로 강화하면서, 현재 거의 모든 스마트폰과 여타 휴대용 전자기기의 커버 윈도우로 사용되는 SAS 유리에는 공히 화학강화 공정이 적용되고 있다.[22]
한편, 유연 디스플레이용 UTG와 더불어 박형화 관련 연구개발이 활발하게 진행되고 있는 자동차용 외부 유리와 인포테인먼트용 대면적 곡면 디스플레이에도 화학강화 유리가 적용되고 있으며, 향후 수요분야가 더욱 확대될 것으로 예상된다. 위에서 언급한 것처럼 산업적 응용을 위한 일반적인 화학강화 방식은 Na+ 이온 함유 유리를 K+ 이온 기반 염욕에 침지하여 이온교환을 유도하는 방식이 적용되고 있으며, 대개의 경우 온도와 시간을 조절하여 표면 압축응력(CS; compressive stress) 및 확산 깊이를 제어하게 된다. 즉, 유리 내부에 존재하는 Na+ 이온과 유리 외부에 존재하는 K+ 이온의 농도 차이로 인한 상호확산이 발생하며, K+ 이온(이온반경 0.133 nm)이 Na+ 이온(이온반경 0.097 nm)보다 더 큰 이온반경을 지니고 있음에 따라 이온교환 영역에서 충진 효과가 발생하여 압축응력이 인가된다. 해당 이온교환은 상호확산에 의해 발생하며, 상호확산계수(D −) 는
압축응력의 분포는 결국 시간 경과에 따른 K+ 이온의 공간적 분포에 의하여 지배되며, 전형적인 습식공정 기반 이온교환의 경우 K+ 이온의 위치(x)와 시간(t)에 대한 농도(C(x,t))는
초박형 유리의 경우 탄성변형에 민감하고 확산 깊이를 자유롭게 제어할 수 없기 때문에 이온교환 공정조건을 최적화하는 것이 더욱 난해하다. 그럼에도 불구하고, 초박형 유리의 효용성을 높이기 위해서는 화학강화가 필수적이다. 고분자 소재의 경우 이온교환을 통한 화학강화 기구를 적용할 수 없기 때문에 변형동작과 관련된 유연성의 평가에 있어 고분자 소재와 UTG에 동일한 평가지표를 적용하는 것이 적절하지 않다. 따라서 UTG를 대상으로 변형의 용이성과 화학강화의 효능성을 동시에 반영하는 관련 성능지수(FOM; figure of merit)의 수립이 필요하다. 이에 본 연구진은 다음과 같은 논의를 바탕으로 UTG의 화학강화 성능지수를 제안하고자 한다. UTG의 화학강화 성능은 유리 내부로 확산되어 들어가는 K+ 이온의 농도(C)와 유리의 두께(t)에 비례하며, 전술한 바와 같이, UTG의 유연성은
침지 기반 이온교환 방식은 태생적으로 연속 공정의 적용이 어려울 뿐만 아니라, 과다한 KNO3 용융염의 사용에 기인하는 NO x 발생 및 위치선택적 이온교환의 적용이 어렵다는 단점이 있다. 비침지 기반 이온교환 방식은 유리를 염욕에 침지하는 대신 알칼리염을 함유하는 슬러리를 제작하여 이를 스프레이 분사 또는 페이스트 도포 공정을 통하여 유리 표면에 막을 형성한 후 후속 열처리를 통하여 이온교환을 발생시킨다.[26] 일련의 건식 이온교환 공정이 제안되어 왔으나, 이온교환 후 발생하는 유리의 의도하지 않은 변형 및 국부적인 결함에 의한 균일성 저하로 인하여 실효성을 인정받지 못하였다.[27] 그러나 위에서 기술한 바와 같이 물리강화 대비 화학강화 방식을 적용하여야 하는 상황이 발생하고 있으며, 나아가 위치선택적 이온교환 공정을 통하여 화학강화의 기능성을 더욱 향상시킬 수 있기 때문에 건식 이온교환 공정에 대한 연구가 필요하다. 특히, ASMG 의 구현은 건식 이온교환 공정의 최적화를 통하여 달성될 수 있다. 잘 알려진 기존의 건식 이온교환 공정에서는 주로 카올리나이트 기반의 점토류 입자를 알칼리염과 함께 물에 혼합하여 만든 슬러리를 활용한다.[28] 그러나 이러한 점토류 입자는 거의 모든 경우에 실리콘과 알루미늄 원자를 포함하는 4성분계 이상의 복잡한 화학양론비를 가지며 층상 구조로 이루어져 있어 수산화기 이온 또는 결정수(crystal water) 분자를 용이하게 함유할 수 있다. 또한, 해당 입자의 크기 및 형태가 균일하지 않아서 슬러리 제작에 있어 균일성과 재현성이 떨어지게 된다. 특히, 해당 점토류 입자들은 SLS 및 SAS 유리의 구성 성분을 포함하고 있기 때문에 이온교환이 발생하는 온도 대역에서 유리 표면과 비가역적인 화학적 반응을 발생시켜서 표면을 오염시키게 된다. 이에 본 연구진은 화학양론비가 단순한 2성분계 금속산화물 나노입자를 활용하여 알칼리염 함유 슬러리를 제작하고, 이를 스프레이 분사 기반 또는 페이스트 도포 기반 공정을 통하여 표면에 막을 형성하고 열처리하여 이온교환을 발생시키는 건식 화학강화 공정을 연구하고 있다. 해당 나노입자는 열처리 온도대역에서 유리 표면과 가시적인 비가역적 화학반응을 발생시키지 않으면서 알칼리 이온의 불필요한 유동을 방지하는 지지체 기능을 수행한다.
이성분계 나노입자 활용 건식 이온교환 공정에 기반한 ASMG 구현 사례를 소개하기 전에 스프레이 코팅과 페이스트 코팅을 통하여 화학강화된 유리의 CS 및 DOL 을 Fig. 8에 전형적인 침지방식으로 화학강화된 유리와 비교하여 도시하였다. 각각의 건식 이온교환 공정은 막 형성 및 후속 이온교환 과정에서 공히 유리를 수직으로 세워 둔 형태로 수행되었다. 전반적으로 기존 습식 화학강화와 비교하여 확산 깊이가 거의 동일하며, 표면 압축응력 역시 큰 차이가 없음을 알 수 있다. 유리 표면에서 발생할 수 있는 결함 및 균일도 저하를 공정조건의 제어를 통하여 해소할 수 있었으며, 나아가 임의의 형상으로 임의의 위치에 선택적인 이온교환이 가능함을 보여주는 사례를 Fig. 9에 도시하였다. 본 사례에서는 세워진 상태의 유리에 삼각형, 사각형 및 원형으로 도포막을 형성한 후 세워진 상태 그대로 건식 이온교환 공정을 진행하여도 도포막의 형상이 유지됨을 확인할 수 있으며, 세척을 통하여 해당 도포막을 제거하면 이온교환 경계선이 육안으로 확인되지 않는 반면에 두 개의 편광판 사이에 유리를 넣어서 확인하면 이온교환이 발생하여 화학강화가 달성된 영역과 그렇지 않은 영역의 경계를 볼 수 있다. 이는 이온교환된 영역의 굴절률이 상승하기 때문이며, 경계선의 육안상 시인성 여부는 위치선택적 이온교환 공정에서 세심하게 제어되어야 한다.
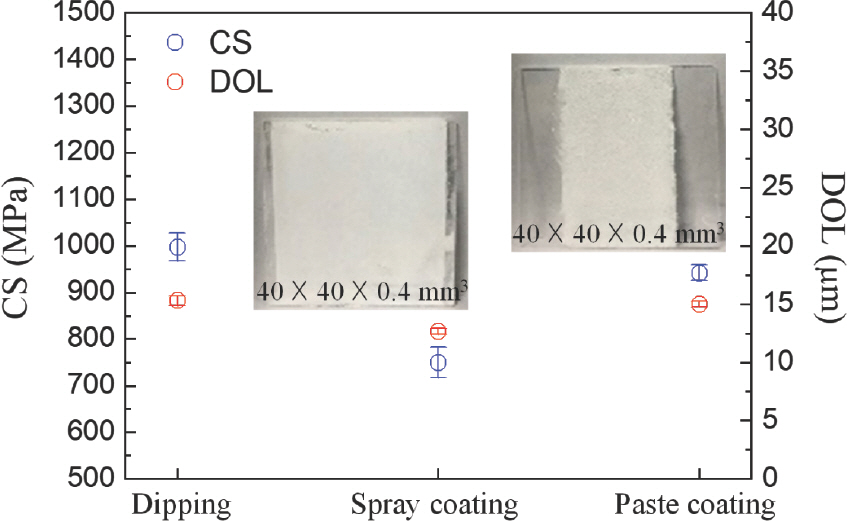
Comparison of CS and DOL values of sodium-aluminosilicate glass (40×40×0.4 mm3 in size) chemically strengthened via different ion exchange processes.
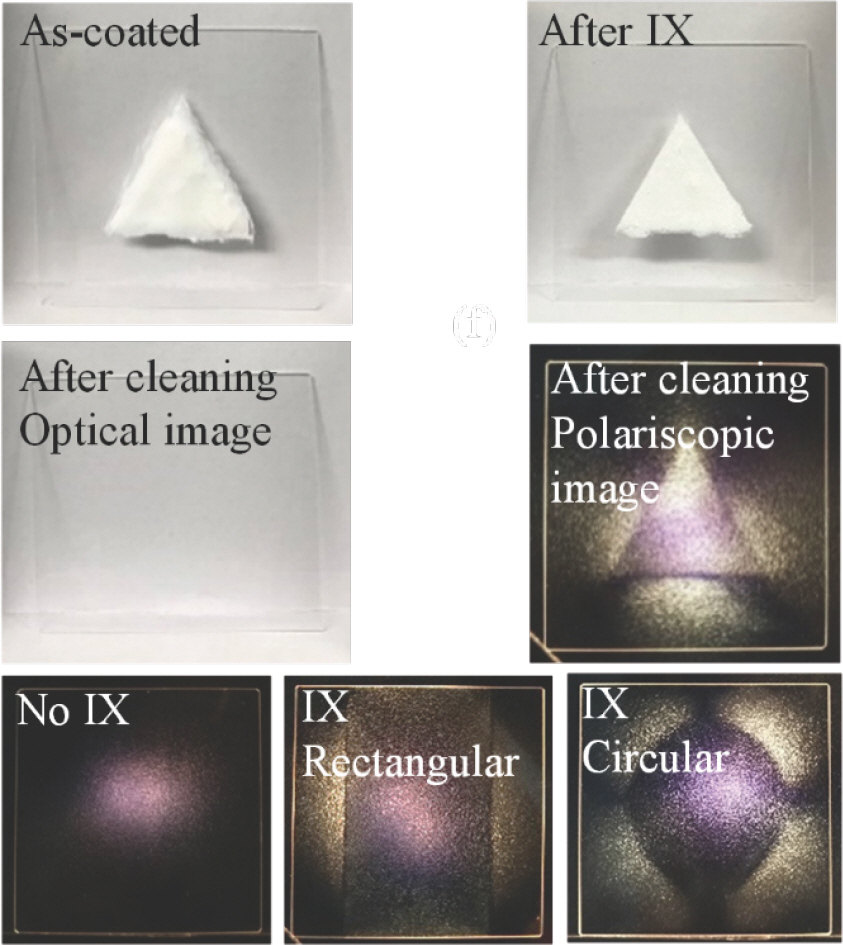
Some exemplary cases of ASMGs embodied by using the non-dipping position-selective ion exchange process. The uneven intensity distribution of transmitted light noticed in the case of the untreated glass is caused by the use of point light source, and therefore has nothing to do with the uniformity of the pristine glass.
한편, 삼각형 형태로 위치선택적 이온교환을 거친 유리의 표면을 위치에 따라 비커스 경도를 측정한 결과를 Fig. 10에 도시하였다. 이온교환이 발생한 위치와 발생하지 않은 위치에서 뚜렷한 경도의 차이를 확인할 수 있으며, 이온교환이 발생한 위치에서 측정한 EDS 결과에서도 전형적인 Na+ 이온과 K+ 이온의 깊이 방향에 대한 농도 분포를 확인할 수 있다. 또한, 교환 영역과 미교환 영역의 경계를 가로질러 유리표면에서 각 이온의 농도 분포를 측정한 결과 연속적으로 농도가 변화함을 확인하였으며, 이를 바탕으로 경계선 부근에서의 굴절률 변화 양상을 유추할 수 있다.
5. 요약 및 제언
유연 디스플레이의 커버 윈도우에 적용되는 초박형 유리는 기존 폴더블 폼 팩터에 성공적으로 적용되었고, 향후 슬라이더블 및 롤러블 형태에도 적용될 수 있도록 각 변형동작의 요구특성에 대한 적합성 관련 연구가 필요하다. 유리 소재의 박형화에 대한 요구는 디스플레이 분야를 포함하여 여타 분야에서도 제기되고 있으며, 이에 따라 기존 물리강화 방식 대비 화학강화 방식이 상대적으로 중요해지고 있다. 특히, UTG의 경우 화학강화를 통하여 유연성 확보에 필요한 두께 의존성을 고분자 소재보다 완화할 수 있게 된다. 또한, 위치선택적 이온교환 공정의 개발을 통하여 유리 소재에 추가적인 기능성을 부여할 수 있을 것이며, ASMG의 구현은 동일 면에서 압축강도의 크기를 변화시키거나 양면 비대칭 강화 효과를 부여하거나 의도적인 소성변형을 유도하는 등의 다양한 방법론을 통하여 유리 소재의 화학강화 효과를 더욱 제고할 수 있을 것이다.
Acknowledgements
본 논문은 정부(산업통상자원부)의 재원으로 소재부품기술개발사업(No. 20015627)의 지원을 받아 수행되었다.
References
Biography

◉◉이지인
◉ 2013-2018년 한국항공대학교항공재료공학과 학사
◉ 2018-2020년 한국항공대학교항공재료공학과 석사
◉ 2020년-현재 한국항공대학교 신소재공학과박사과정

◉◉고세영
◉ 2013-2019년 한국항공대학교항공재료공학과 학사
◉ 2019-2021년 한국항공대학교항공재료공학과 석사
◉ 2021년-현재 한국항공대학교 신소재공학과박사과정

◉◉최용규
◉ 1987-1991년 KAIST 재료공학과 학사
◉ 1992-1994년 POSTECH 신소재공학과 석사
◉ 1994-1998년 POSTECH 신소재공학과 박사
◉ 1998-2004년 한국전자통신연구원원천기술연구본부 선임연구원
◉ 2000년 ORC, Southampton Univ. 영국방문연구원
◉ 2010-2011년 IMI-NFG, Lehigh Univ.미국 방문교수
◉ 2018년 Zhejiang Univ. 중국 방문교수
◉ 2004년-현재 한국항공대학교 신소재공학과조교수/부교수/교수