ņŚ░ļŻīņĀäņ¦ĆļŖö ļŗżņ¢æĒĢ£ ņŚ░ļŻīļź╝(ņłśņåī ļśÉļŖö ĒāäĒÖöņłśņåī Ļ│ä) ņ¦üņĀæ ņĀäĻĖ░ņŚÉļäłņ¦ĆļĪ£ ņĀäĒÖśĒĢĀ ņłś ņ׳ļŖö ņĀäĻĖ░ļ░£ņāØņןņ╣śļĪ£ ņŚÉļäłņ¦Ć ĒÜ©ņ£©ņØ┤ ņāüļŗ╣Ē׳ ļåÆĻ│Ā ņĀäĻĖ░ņāØņé░ ļ░śņØæņØä ĒåĄĒĢ┤ ņāØņä▒ļÉśļŖö ļČĆņé░ļ¼╝ņØ┤ ņśżņ¦ü ļ¼╝ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ņĄ£ĻĘ╝ ļīĆļæÉļÉśļŖö CO2ņŚÉ ņØśĒĢ£ ņ¦ĆĻĄ¼ ņś©ļé£ĒÖöņØś ņĖĪļ®┤ņŚÉņä£ļÅä ņāüļŗ╣Ē׳ ņóŗņØĆ ļīĆņ▓┤ņŚÉļäłņ¦Ć ļ░£ņāØņןņ╣śļØ╝ ĒĢĀ ņłś ņ׳ļŗż. ņØ┤ļ¤¼ĒĢ£ ņŚ░ļŻīņĀäņ¦Ć ņżæņŚÉņä£ ņĢīņ╣╝ļØ╝ņØĖ ņŚ░ļŻīņĀäņ¦ĆļŖö Ļ░Ćņן ņśżļלļÉśĻ│Ā ļ░£ņĀäļÉ£ ņŚ░ļŻīņĀäņ¦ĆļĪ£ņä£ ņŚÉļäłņ¦Ć ĒÜ©ņ£©ņØ┤ ņĢĮ 70%ņŚÉ ļŗ¼ĒĢśļ®░(ņĀäĒĢ┤ņĀäņ¦ĆņØś ņłśņĀäĒĢ┤ ĒÜ©ņ£© ņŚŁņŗ£ ņĢĮ 70%ņŚÉ ļŗ¼ĒĢ©), ņØ┤ļ»Ė ļŗżņ¢æĒĢ£ ļČäņĢ╝ņŚÉ ņŗżņĀ£ļĪ£ ņĀüņÜ®ļÉśņ¢┤ ņé¼ņÜ®ļÉśņ¢┤ņĀĖ ņÖöļŗż.1ŌĆō3) NASAņØś ņĢäĒÅ┤ļĪ£ ņŗ£ļ”¼ņ”ł ļ»ĖņģśņŚÉņä£ 1960ļģä ņżæļ░śĻ╣īņ¦Ć ņĀäĻĖ░ļź╝ ņāØņé░ĒĢśļŖö ņןņ╣śļĪ£ņä£ ņé¼ņÜ®ļÉśņ¢┤ņ¦ä ņØ╝ļĪĆļĪ£ ļ│┤ļ®┤, ņāüļŗ╣Ē׳ ņśżļלņĀäņŚÉ Ļ░£ļ░£ļÉśĻ│Ā ņśżļ×£ ĻĖ░Ļ░äļÅÖņĢł ļ░£ņĀäļÉśņ¢┤ ņÖöņØīņØä ņĢī ņłś ņ׳ļŗż. ĻĘĖļ¤¼ļéś, ļŗżļźĖ ņ░©ņäĖļīĆ ņŚ░ļŻīņĀäņ¦ĆĻ░Ć Ļ┤Ćņŗ¼ņØä ļ¬©ņ£╝ļ®┤ņä£ ņŚ░ĻĄ¼Ļ░£ļ░£ņØś ņåŹļÅä ĒśäņĀĆĒ׳ ņżäņ¢┤ļō£ļŖö ņŗ£ĻĖ░Ļ░Ć ņ░ŠņĢäņśżĻĖ░ļÅä Ē¢łņŚłļŗż. ņśłļĪ£ņä£, proton-exchange electrolyte membrane fuel cells (PEMFC)ņØĆ General ElectricprotonņØś Willard Thomas Grubb Ļ│╝ Leonard NiedrachņŚÉ ņØśĒĢ┤ Ļ░£ļ░£ļÉśņŚłņ£╝ļ®░, ņØ┤ļōżņØĆ sulfonated polystyreneņØś ĻĖ░ņĪ┤ņŚÉ ņĀäĒĢ┤ļ¦ēņØä Nafion ionomerļĪ£ ļīĆņ▓┤ĒĢśļ®┤ņä£ ĒÜ©ņ£©ņØä ņāüļŗ╣Ē׳ Ēü¼Ļ▓ī Ē¢źņāüņŗ£ņ╝░ļŗż. ņĀäĒĢ┤ļ¦ēņØś ņé¼ņÜ®ņØĆ ņŗ£ņŖżĒģ£ņØś Ļ░äņåīĒÖöļź╝ ņØ┤ļüīņŚłĻ│Ā, protonņØś ļ╣ĀļźĖ ņĀäļŗ¼ ņåŹļÅäļĪ£ ņØĖĒĢ┤ņä£ 1960ļģä ņØ┤Ēøä ĻĖ░ņĪ┤ņØś alkaline fuel cell (AFC)ņØä ņé¼ņÜ®ĒĢśļŹś NASAļŖö PEMFCļĪ£ ļīĆņ▓┤ĒĢśĻĖ░ņŚÉ ņØ┤ļź┤ļĀĆļŗż. Anion exchange membraneņØ┤ Ļ│äņåŹņĀüņ£╝ļĪ£ Ļ░£ļ░£ņØ┤ ļÉśņ¢┤ņ¦ĆĻ│Ā ņ׳ņ¦Ćļ¦ī ņāüļīĆņĀüņ£╝ļĪ£ protonļ│┤ļŗż Ēü░ ņØ┤ņś©ļ░śĻ▓Įņ£╝ļĪ£ ņĀäļŗ¼ņåŹļÅäņŚÉņä£ļŖö proton-exchange membraneņŚÉ ņĢäņ¦ü ļ»Ėņ╣śņ¦Ć ļ¬╗ĒĢśĻ│Ā ņ׳ņ¢┤, ļ¦żņÜ░ ņżæņÜöĒĢ£ ņŗ£ņŖżĒģ£ Ļ░äņåīĒÖöņØś ņĖĪļ®┤ņŚÉņä£ Ļ│äņåŹņĀüņØĖ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢ£ ļČäņĢ╝ļØ╝Ļ│Ā ņé¼ļŻīļÉ£ļŗż.
ņé░ņä▒ņĪ░Ļ▒┤ņØś PEMFCņŚÉņä£ļŖö ņĀäĒĢ┤ņ¦łņåŹņØś ļ¦ÄņØĆ proton ņ£╝ļĪ£ ņØĖĒĢ┤ ņāüļīĆņĀüņ£╝ļĪ£ ņé░ņåīĒÖśņøÉļ░śņØæņØś ĒÖ£ņä▒ĒÖö ņŚÉļäłņ¦ĆĻ░Ć Ēü¼Ļ▓ī ņÜöĻĄ¼ļÉśļ®░, ļ░śļīĆļĪ£ ņŚ╝ĻĖ░ņä▒ ņĪ░Ļ▒┤ņŚÉņä£ļŖö ņĀäĒĢ┤ņ¦ł ņåŹņØś ļåÆņØĆ OHŌłÆ ļåŹļÅäļĪ£ Ļ░ĢĒĢ£ OHĻ▓░ĒĢ®ņŚÉ ņØśĒĢ┤ hydrogen oxidation ļ░śņØæņŚÉņä£ņØś activation energyĻ░Ć Ēü¼Ļ▓ī ļéśĒāĆļé£ļŗż.4ŌĆō6) ņłśņĀäĒĢ┤ ļ░śņØæņŚÉ ļīĆĒĢ£ ĻĖ░ļ│ĖņĀüņØĖ ļ¬©ņŗØļÅäļŖö Fig. 1Ļ│╝ Ļ░ÖņØ┤ ļéśĒāĆļé╝ ņłś ņ׳ņ£╝ļ®░, proton-exchange membrane Ļ│╝ anion-exchange membraneņØś ņé¼ņÜ®ņŚÉ ļīĆĒĢ£ ļŗżļźĖ ņłśņĀäĒĢ┤ ļ░śņØæņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ļŗż.
Alkaline electrolysis cells (AEC)ļź╝ ĒåĄĒĢ£ ņłśņĀäĒĢ┤ ļ░śņØæņŚÉņä£ļŖö oxygen evolution reaction (OER)ņŚÉņä£ Ēü░ overpotentialņØä ļ│┤ņŚ¼ņŻ╝ļ®░, ĒÖöĒĢÖļ░śņØæņØĆ ļŗżņØī ņŗØ (1)Ļ│╝ Ļ░ÖņØ┤ ļéśĒāĆļé╝ ņłś ņ׳ļŗż.
ņ┤ēļ¦żņØś ņĖĪļ®┤ņŚÉņä£ ņé┤ĒÄ┤ļ│┤ļ®┤ ļæÉ ņŚ░ļŻīņĀäņ¦Ć ļ░Å ņłśņĀäĒĢ┤ ļ¬©ļæÉ ļ¦żņÜ░ ļé«ņØĆ ņś©ļÅäņŚÉņä£(<100 ┬░C) ņÜ┤ņĀäņØ┤ ļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņåīņØś ņé░ĒÖö/ĒÖśņøÉļ░śņØæĻ│╝ ņé░ņåīņØś ĒÖśņøÉ/ņé░ĒÖöļ░śņØæņØä ņ£äĒĢ┤ platinum (Pt)ņÖĆ Ļ░ÖņØĆ ĒؼĻĘĆĻĖłņåŹņØś ņé¼ņÜ®ņØ┤ Ļ░ĢņÜöļÉ£ļŗż. ņŻ╝ļĪ£ IrO2 ļśÉļŖö RuO2Ļ░Ć ļīĆĒæ£ņĀüņØĖ ņĢīņ╣╝ļØ╝ņØĖ ņĪ░Ļ▒┤ņŚÉņä£ OER ņ┤ēļ¦żļĪ£ņä£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░, ļåÆņØĆ Ļ░ĆĻ▓®ņ£╝ļĪ£ ņØĖĒĢ┤ ņāüņÜ®ĒÖöņŚÉ ļīĆĒĢ£ Ēü░ Ļ▒Ėļ”╝ļÅīņØ┤ ļÉśĻ│Ā ņ׳ļŗż. ļśÉĒĢ£, ņØ┤ļ¤¼ĒĢ£ IrO2ņÖĆ RuO2ļŖö OERļ░śņØæļÅÖņĢł Ļ│╝ņé░ĒÖöĻ│╝ņĀĢņØä ĒåĄĒĢ┤ ņĢīņ╣╝ļØ╝ņØĖ ņĀäĒĢ┤ņĢĪņŚÉ dissolutionļÉśļŖö Ļ▓ĮĒ¢źņØ┤ Ēü¼Ļ▓ī ļéśĒāĆļéś ļé┤ĻĄ¼ņä▒ņØś ņĖĪļ®┤ņŚÉņä£ļÅä ļŗ©ņĀÉņ£╝ļĪ£ ņ×æņÜ®ĒĢ£ļŗż. ĻĘĖļ¤¼ļéś ņé░ņä▒ņĪ░Ļ▒┤ņØś PEMFCņÖĆļŖö ļŗżļź┤Ļ▓ī ņĄ£ĻĘ╝ Ļ░Æņŗ╝ ļŗżņ¢æĒĢ£ ņĀäņØ┤ĻĖłņåŹ/ņĀäņØ┤ĻĖłņåŹņé░ĒÖöļ¼╝ ņ┤ēļ¦żļōżņØ┤ ņŚ╝ĻĖ░ņä▒ ņĪ░Ļ▒┤ņŚÉņä£ ņĢłņĀĢļÉ£ ņä▒ļŖźņØä ļ│┤ņŚ¼ņŻ╝ļŖö Ļ▓āņØ┤ ņĢīļĀżņ¦ÉņŚÉ ļö░ļØ╝ AFC/alkaline electrolysis cells (AEC)ņŚÉņä£ ļŗżņ¢æĒĢ£ ņ┤ēļ¦żļōżņŚÉ ļīĆĒĢ£ ĒŖ╣ņä▒ ļ░Å ņä▒ļŖźņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ļŗżņŗ£ ĒÖ£ļ░£Ē׳ ņ¦äĒ¢ēņØ┤ ļÉśĻ▓ī ļÉśņŚłļŗż. AECņŚÉņä£ oxygen-evolution ņ┤ēļ¦żļōż ņżæ ļīĆĒæ£ņĀüņØĖ Ļ▓āņ£╝ļĪ£ļŖö single metal/ metal oxides, metal-metal alloys, layered double hydroxides (LDH), perovskites, spinel, ĻĘĖļ”¼Ļ│Ā ļŗżļźĖ organometallic ļ¼╝ņ¦łļōżņØ┤ ņ׳ļŗż.
ņĢīņ╣╝ļØ╝ņØĖ ņ┤ēļ¦żņØś ĻĖ░ļ│ĖņĀüņØĖ ĻĄ¼ņĪ░ļŖö Fig. 2ņŚÉņä£ ļ│┤ņŚ¼ņŻ╝ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņĀäņØ┤ĻĖłņåŹ ļśÉļŖö ņĀäņØ┤ĻĖłņåŹ ņé░ĒÖöļ¼╝Ļ│╝ ņ╣┤ļ│ĖņØś ļ│ĄĒĢ®ņ▓┤ļĪ£ ĻĄ¼ņä▒ļÉ£ļŗż. ņ╣┤ļ│ĖņØĆ ņĀäĻĖ░ņĀäļÅäņ▓┤ļĪ£ņä£ ņŚŁĒĢĀņØä ĒĢĀ ļ┐Éļ¦ī ņĢäļŗłļØ╝ ļåÆņØĆ Ēæ£ļ®┤ņĀüņ£╝ļĪ£ ņØĖĒĢ┤ ņ╣┤ļ│Ė ĻĘĖ ņ×Éņ▓┤ļĪ£ņØś ņ┤ēļ¦ż ĒŖ╣ņä▒ņØä ņ¦ĆļŗłĻ│Ā ņ׳ņ¢┤ ļīĆļČĆļČäņØś ņĀĆņś©ĒśĢ ņ┤ēļ¦żņŚÉ ņ¦Ćņ¦Ćņ▓┤ļĪ£ņä£ ĒÖ£ņÜ®ļÉśĻ│Ā ņ׳ļŗż.
ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ ĻĖ░ļ│ĖņĀüņØĖ ņ┤ēļ¦żĻĄ¼ņĪ░ļŖö ļŗżņ¢æĒĢ£ ļ¼ĖņĀ£ņĀÉļōżņØä ļ│┤ņŚ¼ņŻ╝Ļ│Ā ņ׳ļŗż(Fig. 3).8,9) ņ▓½ļ▓łņ¦ĖļĪ£ carbon corrosion ļ¼ĖņĀ£ņØ┤ļ®░, ņĢĮ 0.2 V ņØ┤ņāüņØś ļé«ņØĆ potentialņŚÉņä£ļÅä carbon corrosionņØ┤ ņŗ£ņ×æņØ┤ ļÉĀ ņłś ņ׳ņ£╝ļ®░ ņØ┤ ļ¼ĖņĀ£ņĀÉņØĆ ļåÆņØĆ voltageņśüņŚŁņ£╝ļĪ£ Ļ░łņłśļĪØ ņĀÉņĀÉ Ļ░ĆņåŹļÉ£ļŗż. ņØ┤ļĪ£ ņØĖĒĢ£ Ļ░Ćņן Ēü░ ļ¼ĖņĀ£ņĀÉņØĆ ņ┤ēļ¦żļĪ£ņä£ ņé¼ņÜ®ļÉśļŖö ņĀäņØ┤ĻĖłņåŹļźśĻ░Ć ņ¦Ćņ¦Ćņ▓┤ņØĖ carbonņ£╝ļĪ£ļČĆĒä░ ļ¢©ņ¢┤ņĀĖ ņ┤ēļ¦żņØś ĻĖ░ļŖźņØä ņāüņŗżĒĢśĻ│Ā OERņŚÉņä£ņØś activityĻ░Ć Ēü¼Ļ▓ī Ļ░ÉņåīĒĢśļŖöļŹ░ ņ׳ļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ļŗżņ¢æĒĢ£ ņé░ĒÖöļ¼╝ ņ¦Ćņ¦Ćņ▓┤ļōżņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ¦äĒ¢ēņØ┤ ļÉśĻ│Ā ņ׳ņ¦Ćļ¦ī, Ēśäņ×¼Ļ╣īņ¦ĆļŖö carbonņØä ļīĆņ▓┤ĒĢĀ ļ¦īĒĢ£ ņ¦Ćņ¦Ćņ▓┤Ļ░Ć Ļ░£ļ░£ļÉśņ¦Ć ņĢŖņØĆ ņāüĒā£ņØ┤ļŗż. ņĀüņĀłĒĢ£ ņ¦Ćņ¦Ćņ▓┤ņØś ņĪ░Ļ▒┤ņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØ┤ ļéśņŚ┤ĒĢĀ ņłś ņ׳ļŗż.
1. High electronic conductivity
2. High surface area
3. Strong interaction with metal catalysts
4. Action as a catalyst or a promotor (Minor)
ņØ┤ļ¤¼ĒĢ£ ļ¼ĖņĀ£ņĀÉ ņÖĖņŚÉļÅä ņé░ņä▒ņĪ░Ļ▒┤ņŚÉņä£ ļ│┤ļŗżļŖö ĻĘĖ ņåŹļÅäĻ░Ć ļŖÉļ”¼ļŗżĻ│ĀļŖö ĒĢśņ¦Ćļ¦ī ņŚ¼ņĀäĒ׳ metalņØś dissolutionļ¼ĖņĀ£Ļ░Ć ņĪ┤ņ×¼ĒĢ£ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ņĢīņ╣╝ļØ╝ņØĖ ņłśņĀäĒĢ┤ ņןņ╣śļŖö 6 MņØ┤ņāüņØś ļ¦żņÜ░ Ļ░ĢĒĢ£ ņĢīņ╣╝ļ”¼ ļČäņ£äĻĖ░ņŚÉņä£ ņÜ┤ņĀäņØ┤ ļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ļ¤¼ĒĢ£ metal dissolutionņŚÉ ļīĆĒĢ£ ļ¼ĖņĀ£ļÅä Ļ░£ņäĀņØ┤ ĒĢäņÜöĒĢśļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£ļŖö metal agglomeration ņØ┤ ņ׳ļŖöļŹ░, ņØ┤ļŖö metalĻ│╝ carbonņé¼ņØ┤ņØś Ļ▓░ĒĢ®ļĀźņŚÉ Ēü¼Ļ▓ī ņśüĒ¢źņØä ļ░øļŖöļŗż. OERļ░śņØæņŚÉņä£ redox cycleņØä Ļ▓¬ļŖö ļÅÖņĢł ņĢĮĒĢ£ Ļ▓░ĒĢ®ņØä Ļ░Ćņ¦ĆļŖö metal nanoparticleļōżņØĆ ņä£ļĪ£ Ļ▓░ĒĢ®ĒĢśņŚ¼ ņĀÉņĀÉ Ēü░ ņ×ģņ×ÉĻ░Ć ļÉśņ¢┤Ļ░Ćļ®░ ņ┤ēļ¦żĒÖ£ņä▒ļ®┤ņĀüņØ┤ Ļ░ÉņåīļÉ£ļŗż. ņØ┤ļź╝ ņ£äĒĢ┤ strong metal-support interaction (SMSI)ņØä ĒśĢņä▒ĒĢśĻĖ░ ņ£äĒĢ£ ļ¦ÄņØĆ ņŚ░ĻĄ¼ļōżļÅä ņ¦äĒ¢ēņØ┤ ļÉśĻ│Ā ņ׳ļŖö ņāüĒÖ®ņØ┤ļŗż. ņØ┤ļ¤¼ĒĢ£ ļ¼ĖņĀ£ņĀÉņØä ĒĢ┤Ļ▓░ĒĢśĻĖ░ ņ£äĒĢ£ ĒØÉļ”ä ņżæ ĒĢśļéśļĪ£ņä£ perovskitesļ¼╝ņ¦łņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ĒÖ£ļ░£ĒĢśĻ▓ī ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż.
PerovskiteļŖö ĻĖ░ļ│ĖņĀüņ£╝ļĪ£ ABO3ņØś ĒÖöĒĢÖņŗØņØä Ļ░Ćņ¦ĆļŖö ņé░ĒÖöļ¼╝ņ¦łļĪ£ņä£, ļŗżņØī Fig. 4ņÖĆ Ļ░ÖņØ┤ ļéśĒāĆļé╝ ņłś ņ׳ļŗż. A-siteļŖö ņŻ╝ļĪ£ latticeņØś ņĮöļäłņŚÉ ņ£äņ╣śĒĢśļ®░ alkaline earth ļśÉļŖö rare earth elementsļōżņØ┤ ņ£äņ╣śĒĢ£ļŗż. B-site ļŖö latticeņØś ņżæņŗ¼ņŚÉ ņ£äņ╣śĒĢśļ®░ 3d, 4d, 5d transition metal elementsļōżņØ┤ ņé¼ņÜ®ļÉ£ļŗż.
tļŖö tolerance factor, rAļŖö A-site cationņØś ionic radius, rBļŖö B-site cationņØś ionic radius, ĻĘĖļ”¼Ļ│Ā rO ļŖö anionņØś ionic radiusļź╝ ņØśļ»ĖĒĢ£ļŗż.
Fig.┬Ā4.
Crystal structures of perovskite materials ņØ┤ļ¤¼ĒĢ£ perovskite ĻĄ¼ņĪ░ņØś ĒśĢņä▒/ĒāĆņ×ģ ļśÉļŖö ņĢłņĀĢņä▒ņØĆ tolerance factorņŚÉ ņØśĒĢ┤ ņśüĒ¢źņØä Ēü¼Ļ▓ī ļ░øņ£╝ļ®░ ļŗżņØīĻ│╝ Ļ░ÖņØ┤ ļéśĒāĆļé╝ ņłś ņ׳ļŗż. (2)
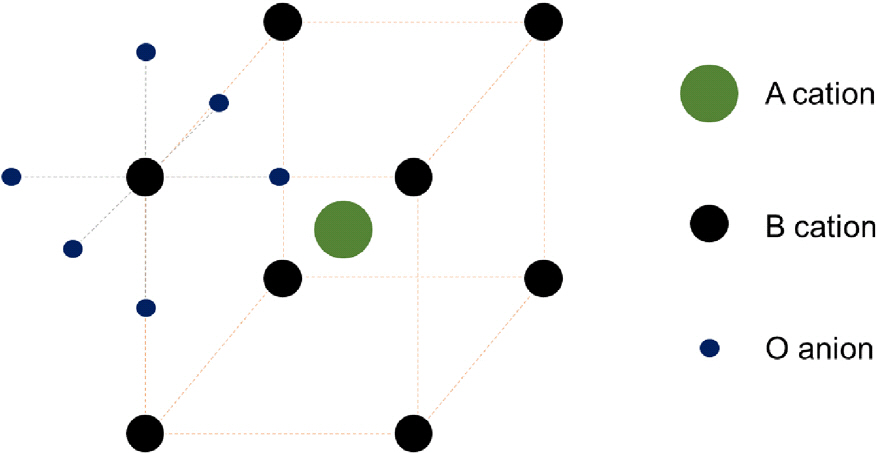
ĻĖ░ļ│ĖņĀüņ£╝ļĪ£ ļåÆņØĆ ļé┤ņé░/ņĢīņ╣╝ļ”¼ ĒŖ╣ņä▒ņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ņ£╝ļ®░, impurityņŚÉ ņØśĒĢ┤ ņĀäĻĖ░ņĀüņØĖ ĒŖ╣ņä▒ņØ┤ Ēü¼Ļ▓ī ļŗ¼ļØ╝ņ¦Ćļ®░, ņĀäņØ┤ ĻĖłņåŹņØä ĻĄ¼ņĪ░ņŚÉ ĒżĒĢ©ĒĢśĻ│Ā ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ļŗżņ¢æĒĢ£ ļČäņĢ╝ņØś ņ┤ēļ¦żļĪ£ņä£ ĒÖ£ņÜ® Ļ░ĆļŖźņä▒ņØ┤ ļ¦żņÜ░ ņ╗ż ņśżļלņĀäļČĆĒä░ ĒÅŁ ļäōņØĆ ļČäņĢ╝ņŚÉņä£ ĒÖ£ņÜ® ļ░Å ņŚ░ĻĄ¼Ļ░£ļ░£ņØ┤ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż. ņØ┤ļ¤¼ĒĢ£ perovskite ĻĄ¼ņĪ░ņØś ņé░ĒÖöļ¼╝ņ¦łņØä ņŚ╝ĻĖ░ņä▒ ņĪ░Ļ▒┤ņŚÉņä£ oxygen-evolution ņŚÉ ļīĆĒĢ£ ņ┤ēļ¦żļĪ£ņä£ ĒÖ£ņÜ®ĒĢśĻĖ░ ņ£äĒĢ┤ ņŗ£ļÅäĒĢ£ Ļ▓āņØĆ ņĄ£ĻĘ╝ņØ┤ ņĢäļŗłļ®░, ņŚ░ĻĄ¼ļōżņØĆ perovskitesņØś activityņŚÉ ļīĆĒĢ£ ņ¦ĆĒæ£ņÖĆ ĒÖöĒĢÖņĀü ņŚ░Ļ▓░ņä▒ņØś ĒÖĢņØĖņŚÉ ņ׳ņŚłļŗż. BockrisdņÖĆ Otagawa ņØś ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤ MOņŚÉņä£ Mz-OHņØś antibonding orbitalņØś occupancyĻ░Ć ņ”ØĻ░ĆļÉśļ®┤ electrocatalytic activityĻ░Ć ņ”ØĻ░ĆĒĢĀ ņłś ņ׳ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.10) RossmeislĻ│╝ Ļ│ĄļÅÖņŚ░ĻĄ¼ņ×ÉļōżņØĆ oxygen ionsĻ│╝ hydroxyl ionsņØ┤ metal/metal oxideņÖĆ Ļ▓░ĒĢ®ĒĢśļŖö Ļ▓░ĒĢ®ņŚÉļäłņ¦ĆļŖö volcano ņÖĆ Ļ░ÖņØĆ ņŚ░Ļ▓░ņä▒ņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ņ£╝ļ®░, binding energyļź╝ ĒåĄĒĢ┤ ļŗżĒ¢źĒĢ£ metal/metal oxideņØś OERņŚÉ ļīĆĒĢ£ activityļź╝ ņśłņĖĪĒĢĀ ņłś ņ׳ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.11) ņĄ£ĻĘ╝ SuntivichņÖĆ Ļ│ĄļÅÖņŚ░ĻĄ¼ņ×ÉļōżņØĆ ļŗżņ¢æĒĢ£ perovskiteļ¼╝ņ¦łņŚÉ ļīĆĒĢ┤ OERļ░śņØæņØä ņĖĪņĀĢĒĢśņśĆĻ│Ā, transition metal ionsņØś Ēæ£ļ®┤ņŚÉ eg orbital ņØś(ņØ╝ļ░śņĀüņ£╝ļĪ£ Žā-bondingņØä Ēæ£ļ®┤ ĒØĪņ░® anionĻ│╝ ĒśĢņä▒) occupancyĻ░Ć OER activityņŚÉ Ēü░ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŗżļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ▓ĮĒ¢źņØĆ ņŚŁņŗ£ volcano plotĒśĢĒā£ļĪ£ ļéśĒāĆļé╝ ņłś ņ׳ņ£╝ļ®░, Ēśäņ×¼ perovskteņØś activity descriptorņżæ ĒĢśļéśļĪ£ ĒÖ£ņÜ®ļÉśĻ│Ā ņ׳ļŗż.12) Jong SukĻ│╝ ĻĘĖ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ perovskitesĻĄ¼ņĪ░ņØś lattice oxygenņØ┤ OER ņŚÉ ņ░ĖņŚ¼ĒĢśļ®░, Ļ░ĆņŚŁņĀüņ£╝ļĪ£ ļ░śņØæņŚÉ ņ░ĖņŚ¼ĒĢśļŖö ņé░ņåī ļ╣łņ×Éļ”¼ļź╝ ĒåĄĒĢ┤ ņØ┤ļ¤¼ĒĢ£ Ēæ£ļ®┤ lattice oxygenņØ┤ OERļ░śņØæņŚÉņä£ņØś intermediated productĒśĢņä▒ņØä ņ┤ēņ¦äĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśĻ│Ā ņ׳ļŗż.13) ņØ┤ļ¤¼ĒĢ£ ņØ┤ļĪĀļōż ņØ┤ņÖĖņŚÉ ļŗżņ¢æĒĢ£ ņØ┤ļĪĀļōżņØ┤ ļ░£Ēæ£ļÉśĻ│Ā ņ׳ļŖö Ļ░ĆņÜ┤ļŹ░, ļŗżņ¢æĒĢ£ perovskiteļ¼╝ņ¦łņŚÉ ļīĆĒĢ£ ņŗżĒŚśņĀü OERļ░śņØæņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļÅä ĒÖ£ļ░£ĒĢśĻ▓ī ņ¦äĒ¢ēņØ┤ ļÉśĻ│Ā ņ׳ļŗż.
Perovskiteļ¼╝ņ¦łņØś catalytic activityļŖö stoichiometry ņŚÉ ņØśĒĢ┤ Ēü¼Ļ▓ī ņśüĒ¢źņØä ļ¦ÄņØ┤ ļ░øļŖöļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ņåīļ¤ēņØś impurityļź╝ ļÅäņ×ģĒĢśņŚ¼ defects (e.g. oxygen vacancy)ļź╝ Ļ░ĢņĀ£ļĪ£ ņāØņä▒ĒĢśņŚ¼ ņ┤ēļ¦żļ░śņØæņŚÉ ļīĆĒĢ£ ņ┤ēļ¦żĒÖ£ņä▒ņĀÉņ£╝ļĪ£ ņØ┤ņÜ®ĒĢśļŖö Ļ▓ĮĒ¢źņØ┤ ņ׳ļŗż. ļśÉĒĢ£, ņØ┤ļ¤¼ĒĢ£ non-stoichiometryņŚÉ ņØśĒĢ┤ ņĀäĻĖ░ņĀü ĒŖ╣ņä▒(e.g. electronic conductivity)ņØ┤ Ēü¼Ļ▓ī ļŗ¼ļØ╝ņ¦ĆĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ļ¤¼ĒĢ£ ļ░®ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĢīņ╣╝ļØ╝ņØĖ ņĪ░Ļ▒┤ņŚÉņä£ ļåÆņØĆ ņĀäĻĖ░ņĀäļÅäņä▒ņØä Ļ░Ćņ¦ĆļŖö support ļ░Å catalystņŚŁĒĢĀņØä ĒĢĀ ņłś ņ׳ļŖö perovskiteļ¼╝ņ¦łņØä Ļ░£ļ░£ĒĢśļŖö Ļ▓āļÅä Ļ░ĆļŖźĒĢś ļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. Non-stoichiometryļź╝ ņØ┤ņÜ®ĒĢ£ ļ¦ÄņØĆ ņŚ░ĻĄ¼ļōżņØ┤ ņ׳Ļ│Ā, ĻĘĖ ņżæ ņĄ£ĻĘ╝ SrIrO3ņ┤ēļ¦żļź╝ ņĀüņÜ®ĒĢśņŚ¼ ļåÆņØĆ OERņä▒ļŖźņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. SeitzņÖĆ ĻĘĖ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ OER cyclingļÅÖņĢł SrIrO3ņŚÉņä£ anatase IrO2Ļ░Ć segregationļÉśņ¢┤ IrO2/SrIrO3ĒśĢĒā£ņØś ļ│ĄĒĢ®ņ▓┤ ĒśĢĒā£ļź╝ ļØäĻ▓ī ļÉśļ®░ ņé░ņä▒ņĪ░Ļ▒┤ņØĆ ļ¼╝ļĪĀ ņŚ╝ĻĖ░ņä▒ ņĪ░Ļ▒┤ņŚÉņä£ ļåÆņØĆ ņä▒ļŖźņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.5) ĒŖ╣Ē׳, ņĢīņ╣╝ļØ╝ņØĖ ņĪ░Ļ▒┤ņŚÉņä£ļŖö IrO2ņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ ļé«ņØĆ overpotentialĻ│╝ ļåÆņØĆ current densityļź╝ ļ│┤ņŚ¼ņŻ╝ņ¢┤ ņāüļŗ╣ĒĢ£ Ļ░£ņäĀņØä ņØ┤ļżäļāłļŗż. ļ¼ĖĒŚīņŚÉ ļö░ļź┤ļ®┤ SrņØś leaching ņØ┤ OER cyclingļÅÖņĢł ļéśĒāĆļé¼Ļ│Ā ņØ┤Ļ▓āņØ┤ 30 minņĀĢļÅä ņ¦ĆņåŹņØ┤ ļÉśņ¢┤ ĻĘĖ ĒøäņŚÉļŖö ĒÅēĒśĢņāüĒā£ņŚÉ ļÅäļŗ¼ĒĢ£ļŗżĻ│Ā ĒĢśņśĆļŗż. Sr ļČäļ”¼ĒśäņāüņØĆ SrIrO3ņØś Ēæ£ļ®┤ĻĄ¼ņĪ░ļź╝ ļ│ĆĒÖöņŗ£ĒéżĻ│Ā non-stoichiometric ĒśĢĒā£ļź╝ ļØäļŖö Sr deficient perovskiteĻ░Ć Ēæ£ļ®┤ņŚÉ ĒśĢņä▒ļÉĀ Ļ▓āņØ┤ļŗż. Alkaline earth metalņØĆ ņĢĪņ▓┤ņāüĒā£ņØś ņĀäĒĢ┤ņĢĪņåŹņŚÉņä£ ņēĮĻ▓ī dissolutionļÉĀ ņłś ņ׳Ļ│Ā ņØ┤Ļ▓āņØĆ alkaline earth metalņØä ņŻ╝ļĪ£ A-siteņŚÉ Ļ░Ćņ¦ĆļŖö perovskiteĻĄ¼ņĪ░ ļ¼╝ņ¦łņŚÉņä£ ņóŗņ¦Ć ņĢŖĻ▓ī ņ×æņÜ®ĒĢĀ ņłśļÅä ņ׳ņØä Ļ▓āņØ┤ļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ┤ĆņĀÉņŚÉņä£ A-site deficient perovskitesļŖö alkaline earth metalņØś ņ╣©ņČ£ĒśäņāüņØä ļ░®ņ¦ĆĒĢĀ ņłś ņ׳ļŖö ĒĢśļéśņØś ļ░®ņĢłņØ┤ ļÉĀ ņłśļÅä ņ׳ņØä Ļ▓āņØ┤ļŗż. ļīĆĒæ£ņĀüņ£╝ļĪ£ solid oxide fuel cells (SOFCs)ņØś Ļ▓ĮņÜ░ ņŻ╝ļĪ£ ņĀäĻĘ╣ļ¼╝ņ¦łņØä perovskiteĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦ĆļŖö ļ¼╝ņ¦łņØä ņé¼ņÜ®ĒĢśļ®░, ĒØöĒ׳ Ļ│Āņś© ņśüņŚŁņŚÉņä£ alkaline earth metalņØś ļČäļ”¼ĒśäņāüņØ┤ ļéśĒāĆļéśļŖö ļ¼ĖņĀ£ņĀÉņØä ļ│┤ņØĖļŗż. ļ¦ÄņØĆ ņŚ░ĻĄ¼ņ×Éļōż ņé¼ņØ┤ņŚÉ A-site Ļ▓░ĒĢ©ņØä Ļ░Ćņ¦ĆļŖö non-stoichiometric perovskitesĻ░Ć ņØ┤ļ¤¼ĒĢ£ ļČäļ”¼ĒśäņāüņØä ļ¦ēņØä ņłś ņ׳ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņŚ╝ĻĖ░ņä▒ ņĪ░Ļ▒┤ņØś OERļ░śņØæņŚÉņä£ ņŚŁņŗ£ ņ¢┤ļŖÉņĀĢļÅä ņĀüņÜ®ņØ┤ Ļ░ĆļŖźĒĢśļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż.
ļśÉ ļö░ļźĖ non-stoichiometric perovskitesņØś ņśłņŗ£ļĪ£ņä£ļŖö BaNiO3Ļ░Ć OERļ░śņØæņØä Ļ▒░ņ╣śļ®░ Ļ▓░ņĀĢĻĄ¼ņĪ░ņØś ļ│ĆĒÖöĻ░Ć ņØ╝ņ¢┤ļéśĻ▓ī ļÉśĻ│Ā non-stoichiometric BaNi0.83 O2.5ĒśĢĒā£ņØś NiņÖĆ O vacancies ĒśĢņä▒ņŚÉ ņØśĒĢ┤ OERļ░śņØæņØ┤ Ēü¼Ļ▓ī Ē¢źņāüļÉĀ ņłś ņ׳ļŗżļŖö Ļ▓āņØä ļ│┤ņŚ¼ņżĆļŗż.6)
Fig. 5ņŚÉņä£ ļ│┤ņŚ¼ņŻ╝ļō»ņØ┤, Ļ▓░ņĀĢĻĄ¼ņĪ░ņØś ļ│ĆĒÖöļĪ£ ņØĖĒĢ┤ Ni-OņØś interatomic distanceĻ░Ć Ōł╝1.92 ├ģņŚÉņä£ Ōł╝1.84 ├ģņ£╝ļĪ£ OER cyclingļÅÖņĢł Ļ░ÉņåīĒĢśļŖö Ļ▓āņØä ņĢī ņłś ņ׳ļŗż. O p-bandņŚÉļäłņ¦Ć ņä╝Ēä░Ļ░Ć Fermi energyļĪ£ Ļ░ĆĻ╣īņÜĖņłśļĪØ OER ĒÖ£ņä▒ļÅäĻ░Ć Ē¢źņāüļÉśļŖö Ļ▓ĮĒ¢źņØ┤ ņ׳ļŗż. ņŗżĒŚśņĀü Ļ▓░Ļ│╝ļōżņØä ļ░öĒāĢņ£╝ļĪ£ ĒĢ£ DFT calculationņŚÉņä£ O p-band energy ņä╝Ēä░ļŖö BaNiO3, BaNiO2, and BaNi0.83 O2.5 ņł£ņ£╝ļĪ£ ŌłÆ2.14, ŌłÆ2.49, and ŌłÆ1.79 eVļĪ£ ļéśĒāĆļé¼ņ£╝ļ®░, BaNi0.83 O2.5Ļ░Ć Ļ░Ćņן ļåÆņØĆ OER activityļź╝ Ļ░Ćņ¦ĆļŖö Ļ▓āņØ┤ ņ¢┤ļŖÉ ņĀĢļÅä ņäżļ¬ģņØ┤ Ļ░ĆļŖźĒĢśļŗż ĒĢĀ ņłś ņ׳ļŗż. ņØ┤ņÖĆ Ļ░ÖņØ┤, non-stoichiometryļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ OER activityļź╝ Ēü¼Ļ▓ī Ē¢źņāüņŗ£Ēé¼ ņłś ņ׳ņØä ļ┐Éļ¦ī ņĢäļŗłļØ╝, ļŹö ļéśņĢäĻ░Ć ņĀäĻĖ░ņĀäļÅäņä▒ļÅä ĒÖĢļ│┤ļź╝ ĒĢśĻ▓ī ļÉ£ļŗżļ®┤ ņ┤ēļ¦żņÖĆ ņ¦Ćņ¦Ćņ▓┤ ņŚŁĒĢĀņØä ļÅÖņŗ£ņŚÉ ĒĢĀ ņłś ņ׳ļŖö multi-functional ļ¼╝ņ¦łņØä Ļ░£ļ░£ĒĢĀ ņłśļÅä ņ׳ļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż.
Fig.┬Ā5.
Difference in OER activity depending on change from BaNiO3 to BaNi0.83 O2.5.14) Copyright ┬® 2016 American Chemical Society
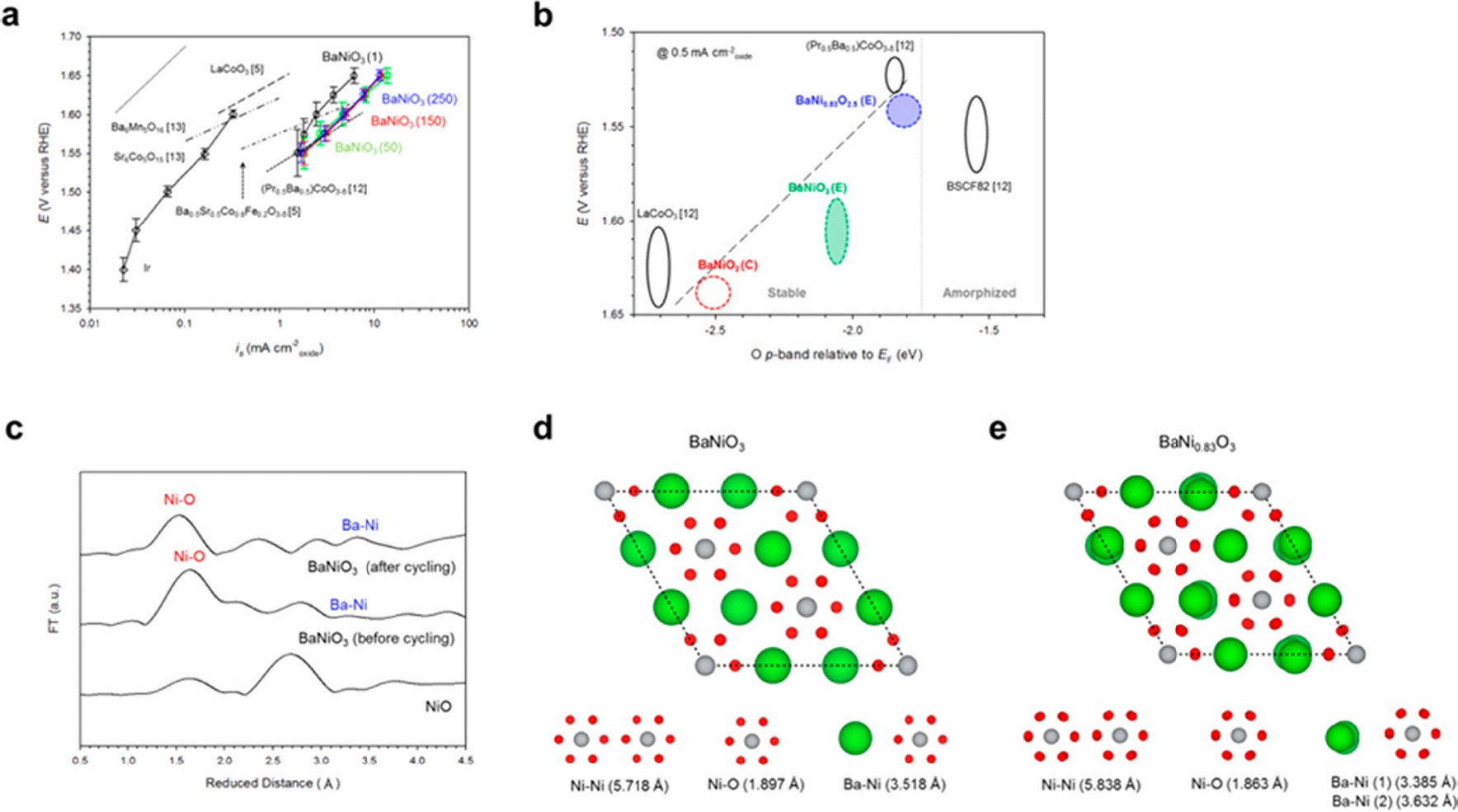
Bifunctional catalystsņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļÅä perovskiteļ¼╝ņ¦łņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ¦ÄņØ┤ ņ¦äĒ¢ēņØ┤ ļÉśĻ│Ā ņ׳ļŗż. YamadaņÖĆ ĻĘĖ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ manganese quadruple perovskites CaMn7 O12ņÖĆ LaMn7 O12ņØś ĒĢ®ņä▒ņŚÉ ņä▒Ļ│ĄĒĢśņśĆĻ│Ā ņØ┤ ņ┤ēļ¦żļōżņØĆ OERĻ│╝ ORRļ░śņØæ ļ¬©ļæÉ ņāüļŗ╣Ē׳ ņóŗņØĆ ņ┤ēļ¦ż ĒÖ£ņä▒ļÅäļź╝ ļ│┤ņŚ¼ņżĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.15) AMnO3Ļ░Ć AMn7 O12ņØś ĒśĢĒā£ļĪ£ Ļ▓░ņĀĢĻĄ¼ņĪ░Ļ░Ć ļ│ĆĒÖöĒĢśļ®┤ņä£ ļåÆņØĆ OER/ORRļ░śņØæņØä ļ│┤ņŚ¼ņŻ╝ļŖö Ļ▓āņ£╝ļĪ£ ņØ┤ ņŚŁņŗ£ non-stoichiometric perovskiteņØś ņóŗņØĆ ņśłņŗ£ļØ╝Ļ│Ā ĒĢĀ ņłś ņ׳ļŗż. ļåÆņØĆ OERņä▒ļŖźņŚÉ ļīĆĒĢ£ ņØ┤ņ£ĀļĪ£ņä£ļŖö AŌĆÖ-ņÖĆ B-siteņØś Mn ionļōżĻ│╝ ņŚ░Ļ▓░ļÉśņ¢┤ ņ׳ļŖö ĒØĪņ░® ļ░śņØæļ¼╝ņé¼ņØ┤ņŚÉ ņ¦üņĀæņĀüņØĖ O-O bondĒśĢņä▒ņ£╝ļĪ£ ņä£ņłĀĒĢśĻ│Ā ņ׳ļŗż. JungĻ│╝ ĻĘĖ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ LaņØ┤ ļÅäņ×ģļÉ£ La x(Ba0.5 Sr0.5)1-x Co0.8 Fe0.2 O3-╬┤ļ¼╝ņ¦łņØä OERļ░śņØæ ņ┤ēļ¦żļĪ£ņä£ ņĀüņÜ®ĒĢśņśĆĻ│Ā, 0.7LaņØś Ļ▓ĮņÜ░ Ļ░Ćņן ļåÆņØĆ ņä▒ļŖźĻ│╝ ņĢłņĀĢņä▒ņØä Ļ░Ćņ¦äļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.16) ņØ┤ļ¤¼ĒĢ£ ļåÆņØĆ ņ┤ēļ¦żĒÖ£ņä▒ļÅäļŖö B-site ņ¢æņØ┤ņś©ņØś electronic structureņÖĆ nano-scale ņĀæĻĘ╝ņŚÉ ņØśĒĢ£ Ļ▓āņØ┤ļØ╝ ņä£ņłĀĒĢśĻ│Ā ņ׳ļŗż. ĒŖ╣Ē׳, nano-scale ņĀæĻĘ╝ļ▓ĢņØĆ ņ┤ēļ¦żĒÖ£ņä▒ļÅäļź╝ Ē¢źņāüņŗ£ĒéżļŖöļŹ░ ļ¦żņÜ░ ĒÜ©ņ£©ņĀüņØĖ ļ░®ļ▓ĢņØ┤ļ®░ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ ņĢĮ 50 nmĒü¼ĻĖ░ņØś ļéśļģĖņ×ģņ×É perovskiteļź╝ ĒĢ®ņä▒ĒĢśļŖöļŹ░ ņä▒Ļ│ĄĒĢśņśĆļŗż. ļåÆņØĆ ļ╣äĒæ£ļ®┤ņĀüĻ│╝ Ēæ£ļ®┤ņŚÉ ĒśĢņä▒ļÉ£ ņłśļ¦ÄņØĆ Ļ▓░ĒĢ©ļōżņØĆ ĒÖĢņŗżĒ׳ ņ┤ēļ¦żĒÖ£ņä▒ļÅäņØś Ē¢źņāüņŚÉ Ēü░ ņŚŁĒĢĀņØä ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņŚ¼Ļ▓©ņ¦Ćļ®░, micro ļśÉļŖö nano ĻĄ¼ņĪ░ņ▓┤Ļ░Ć ņ┤ēļ¦żĒÖ£ņä▒ļÅäņØś Ē¢źņāüņŚÉ Ēü░ ĻĖ░ņŚ¼ļź╝ ĒĢĀ ņłś ņ׳ļŗżļŖö Ļ▓āņØä ļ│┤ņŚ¼ņżĆļŗż. Non-stoichiometric perovskiteņŚÉ ļīĆĒĢ£ ļ¦łņ¦Ćļ¦ē ņśłņŗ£ļĪ£ņä£ KimĻ│╝ ĻĘĖ ņŚ░ĻĄ¼ņ×ÉļōżņØĆ Ca2 Mn2 O3ĒśĢĒā£ņØś oxygen-deficient perovskiteĻ░Ć OERļ░śņØæņŚÉņä£ ļ¦żņÜ░ ĒÖ£ņä▒ļÅäĻ░Ć ļåÆ ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśĻ│Ā ņ׳ļŗż.17) ņØ┤ ņŚ░ĻĄ¼ ņŚŁņŗ£ ņ┤łĻĖ░ņØś ĒśĢĒā£ļŖö CaMnO3ļź╝ ņĘ©ĒĢśĻ│Ā ņ׳ņ£╝ļ®░, ļé«ņØĆ ļåŹļÅäņØś ĒÖśņøÉļČäņ£äĻĖ░ņŚÉ ļģĖņČ£ļÉśņŚłņØä ļĢī, Ca2 Mn2 O3ņØś oxygen-deficient perovskiteĒśĢĒā£ļĪ£ ļ│ĆĒÖöĒĢ£ļŗżĻ│Ā ņä£ņłĀĒĢ£ļŗż. ņāüļŗ╣Ē׳ Ēü░ ļ╣äņ£©ņØś ņé░ņåī ļ╣łņ×Éļ”¼ļź╝ ĒåĄĒĢ┤ ļåÆņØĆ ņä▒ļŖźņØ┤ ļÅäņČ£ļÉĀ ņłś ņ׳ņŚłļŗżĻ│Ā ņśłņāüļÉ£ļŗż.
ņ£äņŚÉņä£ ļ│┤ņŚ¼ņżĆ ņśłņŗ£ļōżĻ│╝ Ļ░ÖņØ┤ perovskiteļ¼╝ņ¦łņØä ĒÖ£ņÜ®ĒĢ£ ņĢīņ╣╝ļØ╝ņØĖ ņĪ░Ļ▒┤ņŚÉņä£ņØś OERļ░śņØæ Ē¢źņāüņØĆ ļ¦żņÜ░ Ēü░ Ļ░ĆļŖźņä▒ņØä ļ│┤ņŚ¼ņŻ╝ļ®░, ĒŖ╣Ē׳ non-stoichiometryņŚÉ ņØśĒĢ£ Ļ▓░ĒĢ©ĒśĢņä▒ņØĆ ņ┤ēļ¦żĒÖ£ņä▒ņØś Ē¢źņāüņŚÉ Ēü░ ņśüĒ¢źņØä ļ»Ėņ╣Ā ņłś ņ׳ļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ļö░ļØ╝ņä£, perovskitesļ¼╝ņ¦łņØä ņ┤ēļ¦żļĪ£ ņäĀņĀĢĒĢĀ ļĢī stoichiometryņØś ņĄ£ņĀüĒÖö ņŚŁņŗ£ Ļ│ĀļĀżļÉśņ¢┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ņé¼ļŻīļÉ£ļŗż. ņØ┤ ņÖĖņŚÉļÅä ļŗżņ¢æĒĢ£ perovskite ĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦ĆļŖö ļ¼╝ņ¦łļōżņØ┤ OERļ░śņØæņØś ņ┤ēļ¦żļĪ£ņä£ ņŚ░ĻĄ¼/Ļ░£ļ░£ļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņłśļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļōżņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż. ņ¢ĖĻĖēļÉśņ¢┤ņ¦ä factorļōż ņØ┤ņÖĖņŚÉļÅä ļ¼╝ņ¦łņØś Ēæ£ļ®┤ņĀü, ņ┤ēļ¦żņØś Ēæ£ļ®┤ facets, ĻĘĖ ņÖĖņŚÉ ļŗżļźĖ ļŗżņ¢æĒĢ£ ņØĖņ×ÉļōżņØ┤ ņ┤ēļ¦żņØś ĒÖ£ņä▒ļÅäņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ņ£╝ļ®░, ņ┤ēļ¦żņØś ņäżĻ│äļ░®ļ▓ĢņØ┤ ļ¦żņÜ░ ņżæņÜöĒĢśļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ļ»ĖņäĖĻĄ¼ņĪ░ņŚÉņä£ ņŚŁņŗ£ perovskiteļź╝ ĒÖ£ņÜ®ĒĢ£ ņ┤ēļ¦żņŚÉņä£ Ēü░ ļČĆļČäņØä ņ░©ņ¦ĆĒĢśļŖöļŹ░ ņØ╝ļ░śņĀüņ£╝ļĪ£ perovskiteļŖö ļåÆņØĆ ņś©ļÅäņŚÉņä£ ĒĢ®ņä▒ņØ┤ Ļ░ĆļŖźĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļ╣äĒæ£ļ®┤ņĀüņØ┤ ņāüļŗ╣Ē׳ ļé«Ļ▓ī ļČäĒżĒĢ£ļŗż. ļö░ļØ╝ņä£ ņĀĆņś©ĒĢ®ņä▒ļ▓Ģ(sol-gel, co-precipitation, ļśÉļŖö hydro/solvothermal)ņŚÉ ņØśĒĢ£ ļ╣äĒæ£ļ®┤ņĀü Ē¢źņāüņØ┤ ņ┤ēļ¦żĒÖ£ņä▒ Ē¢źņāüņŚÉ ņżæņÜöĒĢśļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ņ¦ĆĻĖłĻ╣īņ¦Ć ļ│Ė ĻĖĆņŚÉņä£ ņä£ņłĀĒĢ£ ļé┤ņÜ®ņØĆ OERņŚÉ ļīĆĒĢ£ ĻĖ░ļ│ĖņĀüņØĖ ļ¼ĖņĀ£ņĀÉĻ│╝ perovskite ņ┤ēļ¦żļōżņØś ļŗ©ĒÄĖņĀüņØĖ ņśłņŗ£ļ¦īņØä ļ│┤ņŚ¼ņŻ╝ņŚłņ£╝ļ®░, ņŚ¼ļ¤¼Ļ░Ćņ¦Ć ļŗżņ¢æĒĢ£ ņØĖņ×ÉļōżņØä Ļ│ĀļĀżĒĢśņŚ¼ ĒÖ£ņä▒ļÅäļź╝ ņśłņĖĪĒĢĀ ņłś ņ׳ļŖö ĒĢśļéśņØś ņ¦ĆĒæ£ļĪ£ ļ¦īļō£ļŖö ņŚ░ĻĄ¼Ļ░Ć Ēśäņ×¼ ņĢīņ╣╝ļØ╝ņØĖ ņĪ░Ļ▒┤ņŚÉņä£ņØś OERņ┤ēļ¦żļČäņĢ╝ņŚÉņä£ ņŗ£ĻĖēĒĢ£ Ļ│╝ņĀ£ļĪ£ ņŚ¼Ļ▓©ņ¦äļŗż.












