3차원 나노 다공성 그래핀의 제조와 응용
Three-dimensional Nanoporous Graphene-based Materials and Their Applications
Article information
Abstract
Abstracts
Graphene, a two-dimensional material with a single atomic layer, has recently become a major research focus in various applications such as electronic devices, sensors, energy storage, catalysts, and adsorbents, because of its large theoretical surface area, excellent electrical conductivity, outstanding chemical stability, and good mechanical properties. Recently, 3D nanoporous graphene structures have received tremendous attention to expand the application of 2D graphene. Here, we overview the synthesis of 3D nanoporous graphene network structure with two-dimensional graphite oxide sheets, the control of porous parameters such as specific surface area, pore volume and pore size etc, and the modification of electronic structure by heteroatom doping along with its various applications. The 3D nanoporous graphene shows superior performance in diverse applications as a promising key material. Consequently, 3D nanoporous graphene can lead the future for advanced nanotechnology.
1. 서론
십억 분의 일을 뜻하는 나노는 난쟁이를 의미하는 그리스어 나노스(nanos)를 어원으로 한다. 1 nm는 결국 10−9 m와 같으며 대략 원자 서너 개의 크기에 해당한다. 현대 과학기술은 이러한 나노미터 수준에서 물질의 구조 제어를 가능하게 함으로써 화학 및 재료과학 분야에 무궁한 발전 가능성을 열어주었다. 원자나 분자 수준에서의 이러한 조작은 종종 기존 벌크 소재에서 보지 못했던 새로운 현상을 보여준다. 이러한 신비로운 나노 세계의 근간은 양자 크기 효과(quantum size effect)와 넓은 비표면적(specific surface area)에서 비롯된다. 나노기술은 기존의 독립되어 있던 물리, 전자, 화학 등의 분야가 서로 연결되어 새롭게 구축된 영역으로서 최소의 소비에너지와 크기만으로 최고의 성능을 구현할 수 있는 고도의 경제성을 갖춘 기술이라고 할 수 있다.
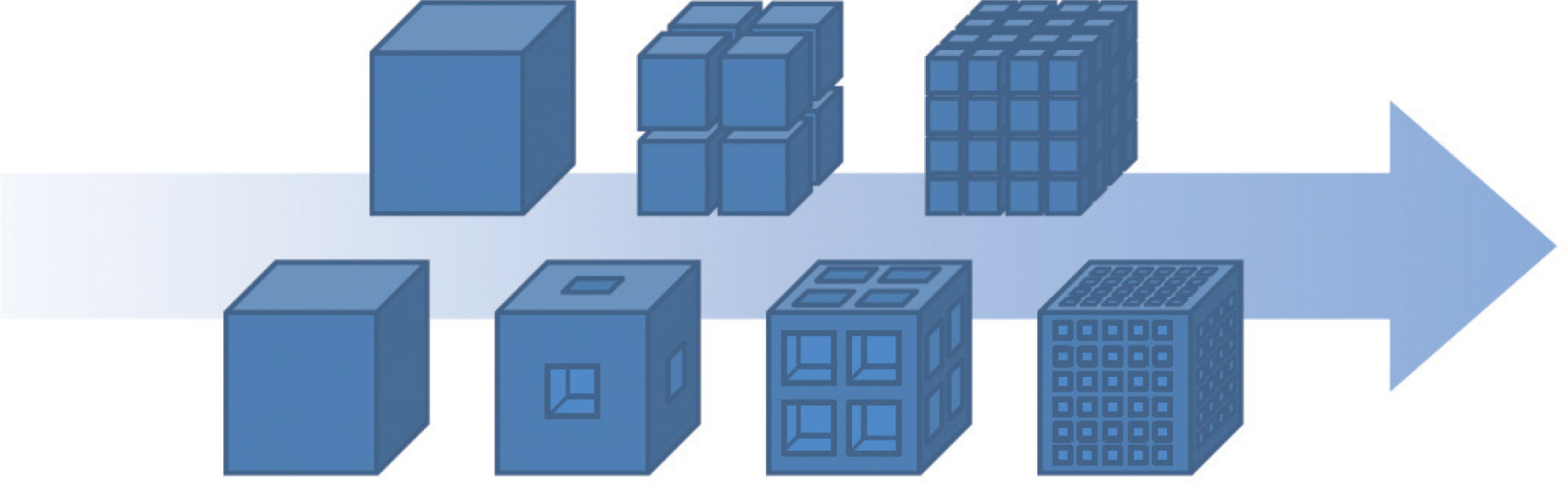
나노물질의 가장 큰 특징은 넓은 비표면적이다. 외부에 노출된 나노물질의 표면을 반응할 수 있는 부분이라고 한다면, 나노물질은 벌크 소재일 때에 비해 훨씬 더 넓은 표면적을 가지기 때문에 반응면에서 유리하다. 예를 들어 정육면체의 입자 하나가 놓여있다고 생각해보자. 한 변의 길이가 10이라면 표면적은 100 × 6을 갖는다. 이때 이 정육면체가 균등하게 8조각으로 나뉜다면 총 표면적은 1,200이 된다. 조각난 크기가 나노미터 단위라면 표면적은 이와 비교되지 않을 정도로 매우 크게 증가할 것이다. 이러한 표면적의 증가는 기공(pore)을 갖는 다공성 물질에도 똑같이 적용할 수 있다. 기공이 생기면서 외부로 노출되는 면적이 증가하게 되므로 기공이 많아지면 표면적도 증가한다(Fig. 1). 표면적의 증가를 정량화하기 위해 비표면적이라는 용어를 사용하는데, 이는 일반적으로 단위 질량당 표면적(m2/g)으로 나타낸다. 따라서, 단순한 입자의 경우 입자 크기를 제어하여 비표면적을 증가시킬 수 있으며, 다공체의 경우 기공 크기를 적절히 변화시켜 제어할 수 있다.
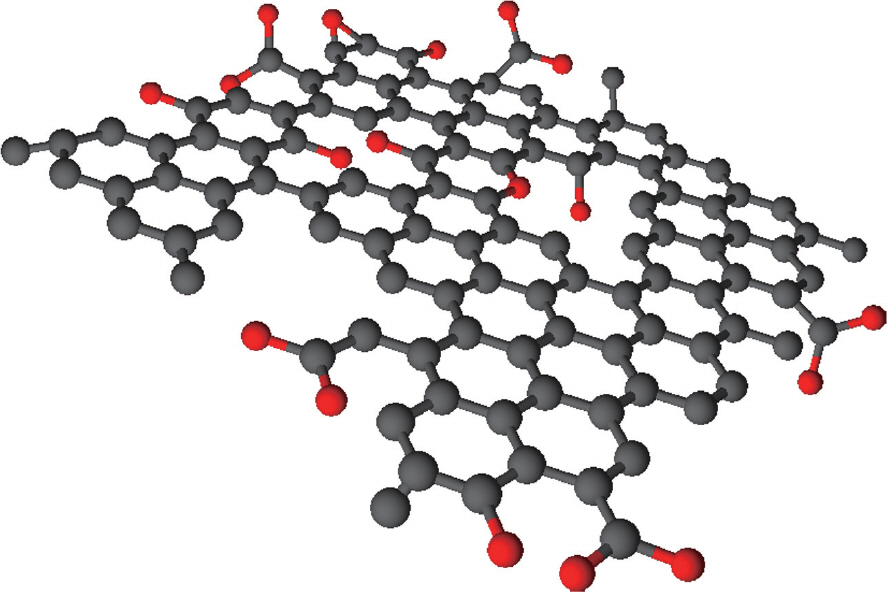
나노기술과 접목되어 다양한 변신을 할 수 있는 물질의 대표적인 예가 그래핀이다. 그래핀은 이론적인 비표면적 이 넓으며, 기계적 강도가 우수하고 전자 이동도와 열전도도가 높다.1) 그래핀의 구조는 탄소 원자가 평면상에 육각형으로 배열된 단일 층으로 이루어져 있으며, 층 내부(in-plane)의 탄소 원자는 주변의 3개의 탄소 원자와 공유결합을 이룬다. 이에 반해, 그래핀과 동소체(allotrope) 관계인 흑연은 단일 층의 그래핀들이 층에 수직인 방향 (out-plane)으로 반데르발스 인력(Van der Waals interaction)이 작용하여 서로 적층된 구조를 가진다. sp2 혼성을 가지는 그래핀은 결합에 참여하지 않은 전자가 p z 오비탈에 채워져 층 전체에 구름처럼 퍼져 있어(비 편재화, delocalization) 높은 전기 전도성을 가지게 된다. 반면, 흑연은 전자가 층에 수직인 방향으로는 전달되기 어려워 전도성이 그래핀보다 낮으며, 층과 층 사이에 작용하는 인력이 약하기 때문에 강도도 상대적으로 낮다. 따라서 흑연으로부터 단일 층의 그래핀을 얻어 그래핀 소재의 나노 복합체를 합성하여 소재의 효율을 향상시키려는 연구가 계속 진행되어왔다. 화학적 박리화(chemical exfoliation)를 이용하여 흑연의 층과 층 사이의 인력을 끊어 그래핀을 얻는 제조법이 제시되었는데, 산화된 흑연(graphite oxide, GO)은 층 사이의 인력이 약해져 쉽게 단일 층으로 박리화되고 다시 환원 과정을 통해 그래핀을 얻을 수 있다(Fig. 2).2,3) 이 방법은 그래핀을 대량으로 생산하기 쉬울 뿐만 아니라 산소가 포함된 작용기가 풍부하여 기능화(functionalization)로 다양한 복합체를 형성할 수 있다. 따라서 GO는 그래핀 기반의 나노 복합체 소재를 만드는데 전구체로 쓰일 수 있다.
다공성 물질은 기공의 직경에 따라 미세기 (micropore), 메조기공(mesopore), 그리고 거대기공(macropore)으로 나뉜다. 다공성 물질은 비표면적이 매우 크고, 기공을 통한 이온이나 전자의 확산이 쉽고 빠르다는 장점을 가진다. 따라서 다공성 물질들은 이온 교환, 선택적 흡착 및 분리, 다양한 촉매 반응 등에 폭넓게 사용된다. 기공이 작을수록 혹은 클수록 좋다고 일반화하기 어려우며, 연구목적과 대상에 따라 적절한 크기의 기공을 제어하는 것이 중요하다. 본론에서는 다공성 물질의 정의와 분류에 대해 우선적으로 소개할 것이다. 다음으로 3차원 나노 다공성 그래핀의 제조와 기공 특성 제어 및 응용성에 대해 기술하고자 한다.
2. 본론
2-1. 나노 다공성 물질의 정의와 분류
나노기술의 발달과 더불어 나노 다공성 물질에 대한 관심도 함께 증가하고 있다. 나노 다공성 물질이란 나노미터 크기 수준의 기공(pore)을 다량 형성하고 있는 물질을 의미한다. 이러한 물질들이 갖는 높은 비표면적으로 인하여 전통적으로 촉매, 흡착제 또는 담체 물질로 응용되어 왔고 최근에 BT(Bio technology), ET(environmental technology), IT(information technology)와 결합하여 그 중요성이 증가하고 있다. 보다 구체적으로, 지능형 약물전달 시스템이나 생화학 반응검출 등의 화학/바이오 센서 분야, 특정물질의 선택적 분리 및 흡착반응을 통해 분자 인식기능을 갖는 환경오염 측정 및 제거 분야, 에너지 절약, 에너지 저장, 에너지 변환 소재, 화학적/전기화학적 활성 소재, 나노 크기의 기공과 높은 비표면적을 최대한 활용할 수 있는 초고용량 커패시터 및 휴대용 연료전지 분야 등의 소재 개발을 위한 핵심기술로 중요하게 인식되고 있다.
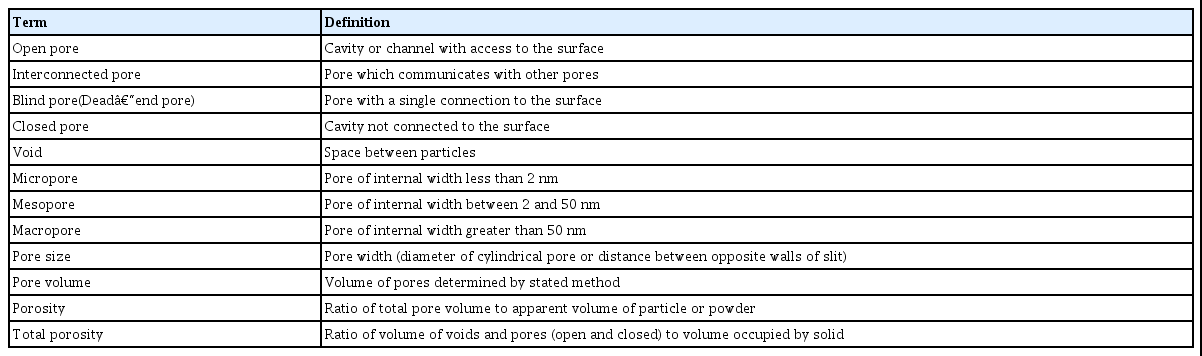
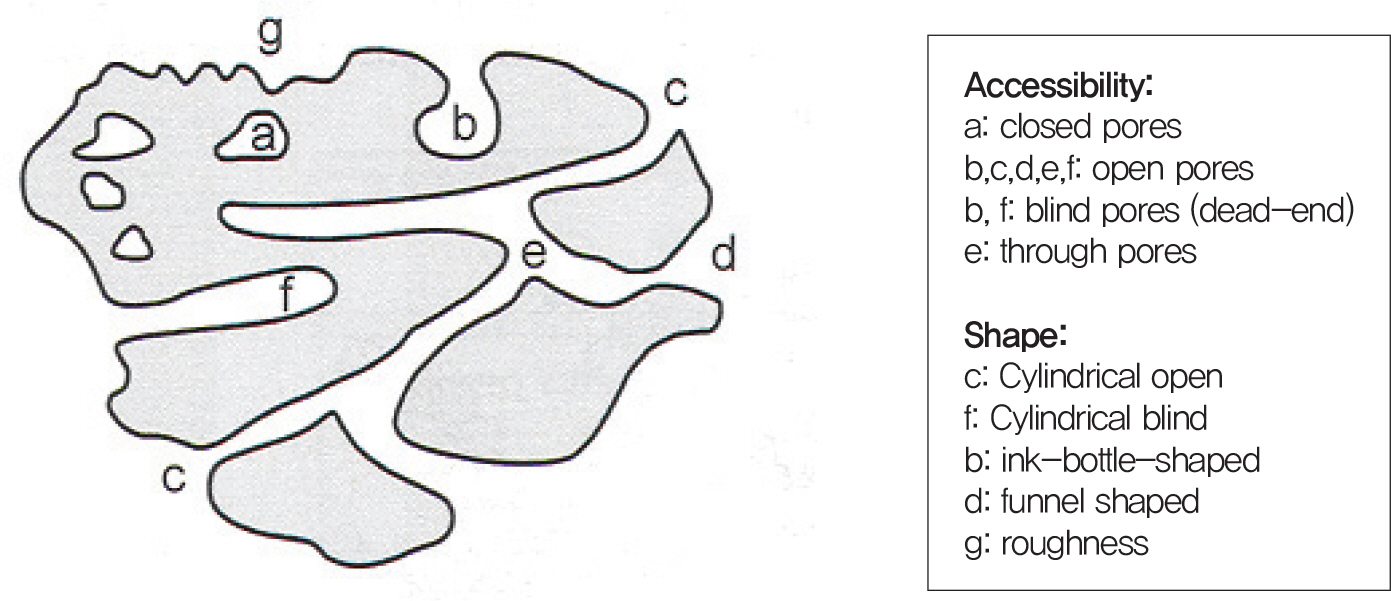
다공성 물질을 분류하는 방법에는 여러 가지 방법이 있으나 일반적으로 기공 크기에 따라 분류하는 IUPAC (international union of pure and applied chemistry) 기준을 따른다. IUPAC 기준에 의하면 그 기공 크기가 2 nm 이하를 미세기공, 2~50 nm의 범위를 메조기공, 그리 고 50 nm 이상을 거대기공으로 구분하고 있다. 다공성 물질에서 존재할 수 있는 일반적인 기공에 대한 정의와 모식도가 Table. 1과 Fig. 3에 나타나 있다.
기공은 크게 닫힌 기공(closed pore)과 열린 기공(open pore)으로 나눌 수 있다. 닫힌 기공이란 기공이 외부와 격리되어 고체 내부에만 고립된 기공을 뜻하고 열린 기공이란 외부와 연결된 상태의 기공을 뜻한다. 따라서 실제 응용적 측면에서 보다 의미 있는 기공은 열린 기공이라고 할 수 있다. 좀 더 세밀히 나누어 보면 기공의 입구와 출구가 같은 막힌 기공(blind pore), 입구와 출구가 다른 즉, 고체를 통과하는 관통 기공(through pore) 등으로 나눌 수 있다. 기공의 모양 측면에서 보면 기공의 입구 부분과 안쪽의 기공 크기의 변화가 없는 원통형(cylindrical) 기공과 좁은 입구와 넓은 내부를 가지고 있는 잉크병 모양(ink-bottle-shaped) 기공 등으로 나눌 수 있다.4,5,6)
2-2. 3차원 나노 다공성 그래핀의 특성
그래핀과 그 유도체는 고유한 특성 때문에 많은 분야에서 관심을 받고 있다. 그래핀은 높은 이론적인 비표면적(2,600 m2/g)과 우수한 전기 전도도 (100 S/m), 전하 이동도(200,000 cm2/Vs), 영률 (~1.0 Tpa), 열전도도 (~5000 W/mK), 광 투과율(97.7%)의 특징을 가진다.1,7) 따라서 나노 다공성 그래핀, 이종 원소가 도핑된 그래핀, 금속 산화물-그래핀 나노 복합체 등과 같은 그래핀 기반 물질들은 전자 및 광전자 소자, 에너지 저장, 화학 센서, 촉
매, 흡착제 등의 응용 분야에서 우수한 특성을 나타낸다. 특히, 기공들이 잘 연결된 3차원 나노 다공성 그래핀은 각 응용 분야에서 보다 우수한 특성을 나타낼 수 있다. 결함(defect)이 없는 순수한 그래핀은 비가역적인 자기응집 현상(self-aggregation)이 나타나기 때문에, 이러한 자기응집을 감소시키기 위해 3차원 다공성 그래핀 구조를 형성시키는 것을 전략으로 할 수 있다. 또한, 다공성 물질은 전자 및 이온의 확산이 빠르기 때문에 에너지 전환 및 저장 장치와 같은 전기화학적인 응용에도 유리한 측면을 가진다. 이처럼 자기응집 현상이 감소된 3차원 나노 다공성 그래핀은 상대적으로 더 넓은 비표면적을 가지며 기공 특성 제어를 통해 위치 및 크기 선택성의 특징 또한 가질 수 있게 된다.11,12,13)
이뿐만 아니라 화학적 도핑(chemical doping)을 이용해서 그래핀의 전기적 성질을 조절할 수도 있다. 화학적 도핑에는 보통 두 가지 접근 방법이 있는데, 하나는 가스, 금속, 유기 분자를 그래핀 표면에 흡착하는 방법이며 다른 하나는 이종 원소(heteroatom)를 치환하는 방법이다. 두 방법 모두 그래핀의 전자 구조 (electronic structure)을 변화시킬 수 있다. 이종 원소 도핑으로는 탄소와 원자 크기가 비슷한 붕소(B), 인(P), 질소(N)가 주로 연구되어 센서나 흡착제, 에너지 저장 물질 및 촉매 등에서 응용되어왔다. 붕소의 원자 크기는 0.088 nm로 탄소 원자 크기(0.077 nm)보다 크기 때문에 graphitic domain에 이종 원소가 치환되게 되면 이웃한 위치에 결함이 발생하므로 그래핀 표면의 활성 자리(activation site)가 유도된다. 이에 더불어 3차원 다공성 구조는 서로 잘 연결된 구조이기 때문에 전자 및 전해질 이온이 기공 사이로 빠르게 이동할 수 있어 에너지 변환 및 저장 장치의 전극 소재로 우수한 특성을 기대할 수 있다.8,9)
2-3. 3차원 나노 다공성 그래핀의 제조와 기공 특성 제어
기공의 역할은 우리가 생각하는 일반적인 개념과 쉽게 연결 지을 수 있다. 비표면적이 크며 기공 크기에 맞는 물질을 선택적으로 받아들일 수 있고, 3차원 다공성 구조는 작은 물질들의 구불구불하고 긴 통로 역할을 할 수 있다. 또한 우수한 전기 전도성을 가지고 있기 때문에 다공성 탄소 물질은 현대 과학기술에 중요한 부분을 차지한다. 다공성 탄소 물질들[활성탄(activated carbon), 카본 블랙(carbon black), 유리 상 탄소(glassy carbon) 등]은 소수성 분자와의 흡착 및 분리, 전극 소재에 용이하다. 그래핀의 이론적인 비표면적은 2,600 m2/g이지만 단일 층 사이의 π-π 상호인력에 의해 다시 쌓이거나(restacking) 혹은 그래핀 단일 층이 구부러지고 접히게 되어 예상한 비표면적 이론값보다 훨씬 감소하게 된다. 따라서 그래핀 층 간의 인력을 적절히 조절하여 3차원 구조의 다공성 그래핀을 제조함으로써 응집 현상을 감소시켜 더 높은 비표면적 값을 가질 수 있다(Fig. 4).
또한 3차원 나노 다공성 그래핀 구조의 기공은 전해질 이온의 통로 역할을 하므로 전해질과 전극 계면 사이의 이온 교환 및 전극 내 전자의 이동이 수월하여 슈퍼커패 시터나 배터리의 전극 소재로 유망하다. 더불어 금속산화물 나노입자를 도입하거나 이종 원소의 도핑 등을 통해서 그래핀의 전기적 성질을 향상시킬 수 있어 차세대 기능성 소재로서 다양한 응용이 가능하다.
3차원 다공성 구조의 그래핀을 만들기 위해서 hard 또는 soft-주형(template)을 활용하는 방법을 주로 이용한다. Hard-주형법을 사용하는 방법에는 구형의 고분자를 이용한 방법, 금속 산화물 나노입자를 이용하는 방법, 그리고 니켈 폼과 같은 다공성 기질을 이용한 방법 등이 사용되었다. 그러나 이와 같은 hard-주형법은 과정이 복잡할 뿐만 아니라 주형을 완전히 제거하는 것이 어려워 실용적인 면에서 제한이 따른다.10,11,12)
반면, soft-주형법은 계면활성제 분자가 자기 조립(self-assembly)되어 만들어진 마이셀 주형을 이용하여 기공 크기가 조절된 물질을 합성할 수 있으며, 상대적으로 주형 제거가 쉬워 최근 활발한 연구가 진행되고 있다. GO는 산소가 포함된 작용기를 가지고 있어 주형의 친수성 부분과 수소 결합, 극성-극성 및 반데르발스 인력을 통해 자기 조립하여 메조 구조체(mesostructured materials)를 형성할 수 있다. 메조 구조체에서 적절한 방법으로 주형을 제거하면 메조 다공성 그래핀(mesoporous graphene, MG)을 얻을 수 있다.13,14,18)
GO와 soft-주형 마이셀 사이의 메조 구조체 형성 과정에서, GO 층과 마이셀 사이에 작용하는 화학적 인력(chemical linkage)을 조절하여 최종적으로 MG의 기공 크기를 제어하는 메커니즘을 설명할 수 있다.3) GO의 하이드록실기 혹은 카복실기 등 산소가 포함된 작용기는 분자 내 혹은 마이셀과 탈수 반응을 통한 올레핀 결합 혹은 에터나 에스터 등의 공유 결합을 형성하기도 한다.4,5)
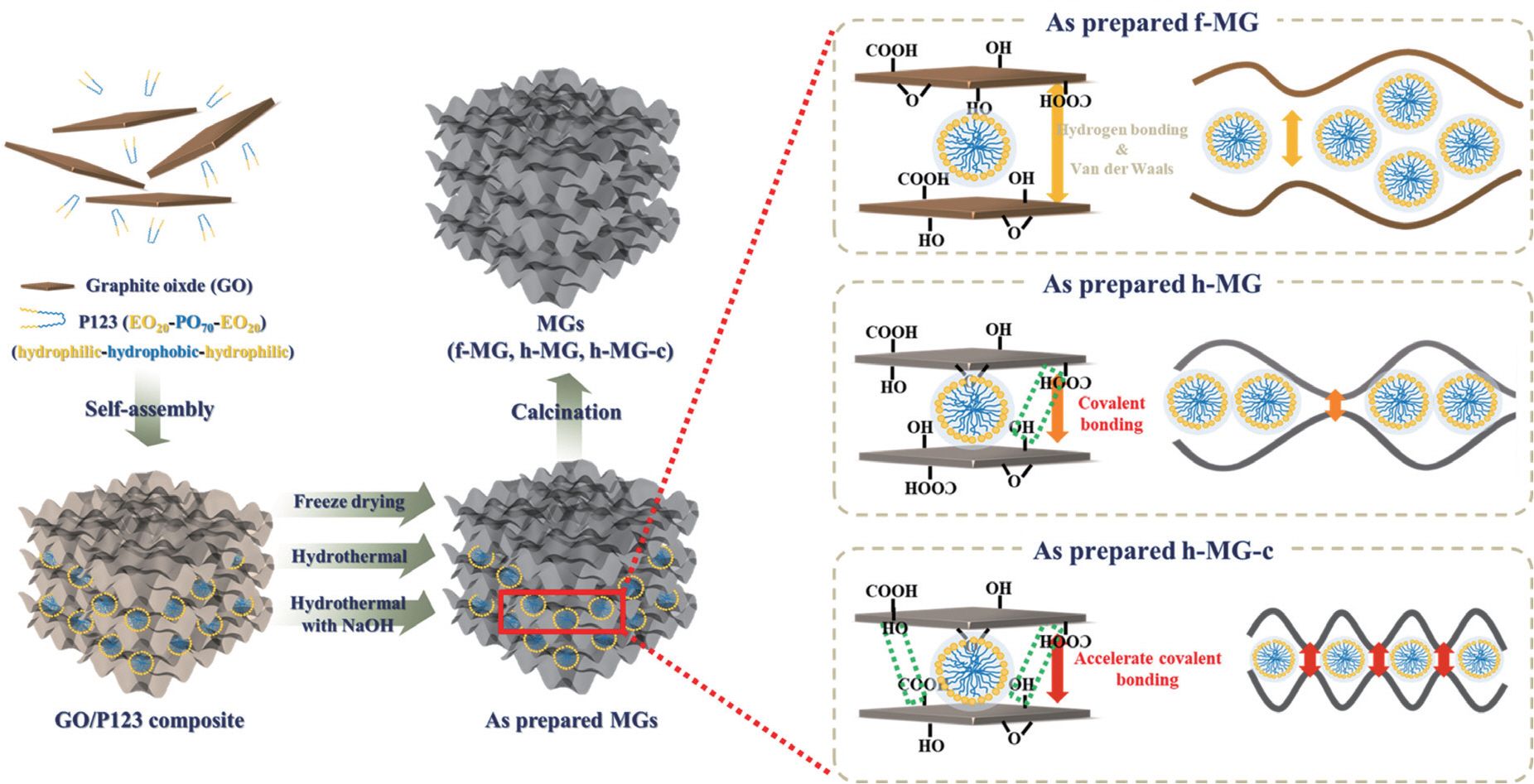
MG의 기공 특성을 변화시키기 위해 합성 방법과 촉매의 유무에 따라 GO 층 사이에 작용하는 화학적 인력의 정도를 조절하여 기공 특성을 제어한 메커니즘이 발표된 바 있다(Fig. 5).15) 합성과정에서 얻어진 메조 구조체 겔의 건조 방법에 따라 기공 특성을 변화시킬 수 있는데, 동결 건조법(freeze drying method)을 이용한 MG(f-MG)는 GO 층간 인력이 주로 수소결합 및 반데르발스 인력에 의해 이루어지므로 기공이 불규칙하고 상대적으로 크게 (11.2 ± 8.7 nm) 만들어진다. 그러나 수열 합성법(hydrothermal method)을 이용한 MG(h-MG)는 층 간의 공유결합 정도가 증가하여 더 작고 균일한 기공(5.0 ± 3.7 nm)을 가질 수 있으며 특히 NaOH와 같은 염기 촉매 하에서 그래핀 표면에 생성된 하이드록실기가 이 반응을 더욱 촉진하여 더 균일하고 작은 기공 크기(3.9 ± 1.7 nm)의 MG(h-MG-c)가 합성될 수 있다. 또한 비표면적 값을 비교하였을 때, 기공 크기가 감소함에 따라 미세기공의 증가로 인한 비표면적 증가 역시 확인할 수 있다(f-MG: 746 m2/g, h-MG: 881 m2/g, h-MG-c: 906 m2/g). 이와 같이 수 nm 범위에서 기공 특성이 제어된 MG는 다양한 응용 분야에 적용될 수 있으며, 제어된 기공 크기 및 기공의 균일도는 모양 및 크기 선택성(shape and size selectivity)과 연결 지을 수 있다.
3. 나노 다공성 그래핀의 응용 가능 분야
3-1. 수소 발생 반응에서의 전기 촉매
수소는 차세대 에너지원으로써 높은 에너지 밀도(140 MJ/kg)를 가진다. 물의 전기분해에 의한 수소 발생 반응(hydrogen evolution reaction, HER)은 촉매 효율을 향상시키기 위해 수소 발생 과정의 과전압을 극복할 수 있는 촉매를 필요로 한다. 효율적인 전기 촉매로 주로 값비싼 귀금속과 그 합금이 사용된다.15)
따라서, 저렴한 가격대비 높은 효율의 전기 촉매를 합성하기 위해서 탄소 기반의 metal-free 촉매를 합성하는 것이 중요하다. 특히 그래핀에 질소나 인과 같은 이종 원소를 도핑하여 최외각 오비탈 에너지에 영향을 줌으로써 인접한 탄소를 활성화시켜 HER의 반응성을 증가할 수 있다.16) 일반적으로 촉매의 다공성은 HER에서 중요한 역할을 한다. 전형적인 가스 발생 불균일 촉매에서, 넓은 비표면적에서 비롯되는 기공 가장자리의 계면에는 많은 촉매 활성 자리가 노출되어 있어 촉매 반응의 효율이 향상된다.10,11)
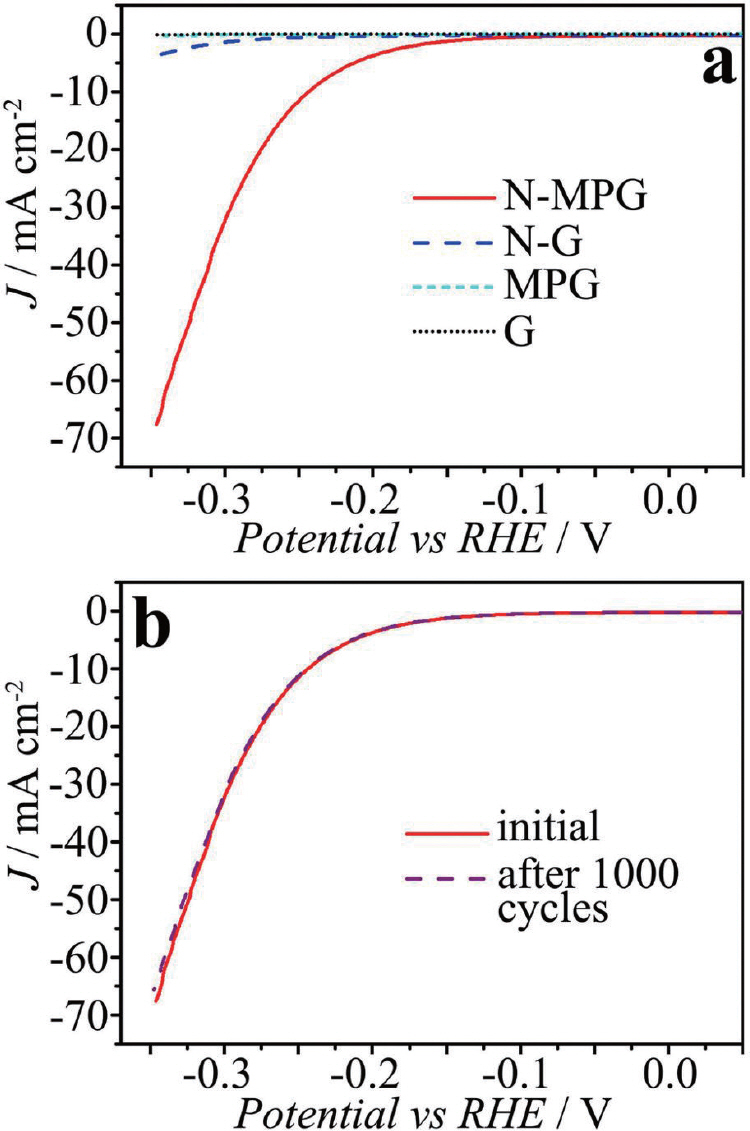
질소가 도핑된 메조 다공성 그래핀(nitrogen doped 3D-mesoporous graphene, NMG)은 특히 비금속 촉매로써 수소 발생 반응에서 효율이 우수하다. 높은 비표면적 값(916 m2/g)을 가지고 있으며 질소 도핑에 의해 활성 자리가 증가하여 HER 전기 촉매로써 우수한 특성을 나타내었다. 수소 원자와 그래핀 사이의 인력은 질소가 도핑됐을 때 더 강하게 작용하였으며 질소 주변의 탄소 원자의 전하 분배(charge distribution) 비대칭에 의해 더 큰 편극(polarization)이 나타났다.
결과적으로, NMG는 최외각 오비탈 에너지 준위가 변해 그래핀의 활성 자리로 이동하는 전자를 가속화하여 흡착된 수소 원자를 수소 분자로 빠르게 변환시킬 수 있다. 따라서 NMG는 전류밀도 10 mA/c m2에서 비금속 촉매 중 가장 낮은 과전압인 239 mV의 값을 가져 우수한 HER 특성을 나타냈다(Fig. 6).17,18)
효율적인 전기 촉매를 구현하는데 있어 NMG의 기공 특성을 제어하는 것 역시 중요하다. 기공 특성의 제어는 모양과 크기 선택성 그리고 화학종의 투과를 위해서 필요하다. 이러한 특징은 수소 발생 뿐만 아니라 다양한 분자의 흡착으로 응용 범위를 넓힐 수 있다.21,22)
3-2. 메조 다공성 그래핀 흡착제
휘발성 유기 화합물(volatile organic compounds, VOCs)은 새집증후군의 주원인으로, 빌딩이나 건축물들 내부의 공기 질을 악화 시켜 두통 및 어지러움을 호소하게 하며 호흡계 질환 및 면역계 질환 등을 일으킬 수 있다. 세계보건기구(world health organization, WHO)에서는 이러한 실내 대기오염물질(indoor air pollutants)의 질병과의 연관성에 주목하고 있어 실내 대기오염물질 감소의 중요성을 언급하고 있다. 활성탄, 제올라이트(zeolite) 등의 다공성 물질들이 VOCs의 흡착제로 많이 사용되고 있다.19)
하지만 기공 크기의 제한이나 흡착제와 흡착질의 충분한 인력이 없어 이러한 물질들의 효율성이 제한되고 있다. 이론적으로 이중 결합을 가지고 있는 그래핀 기반 물질들은 VOCs 분자와 π-π 상호작용을 할 수 있다. 하지만 일반적으로 GO의 환원으로 얻어진 RGO(reduced graphite oxide)의 경우 대부분 2 nm 이하의 미세기공을 가져 폼알데하이드나 벤젠, 톨루엔과 같은 작은 VOCs 분자들의 제거에만 효과적이다.20)
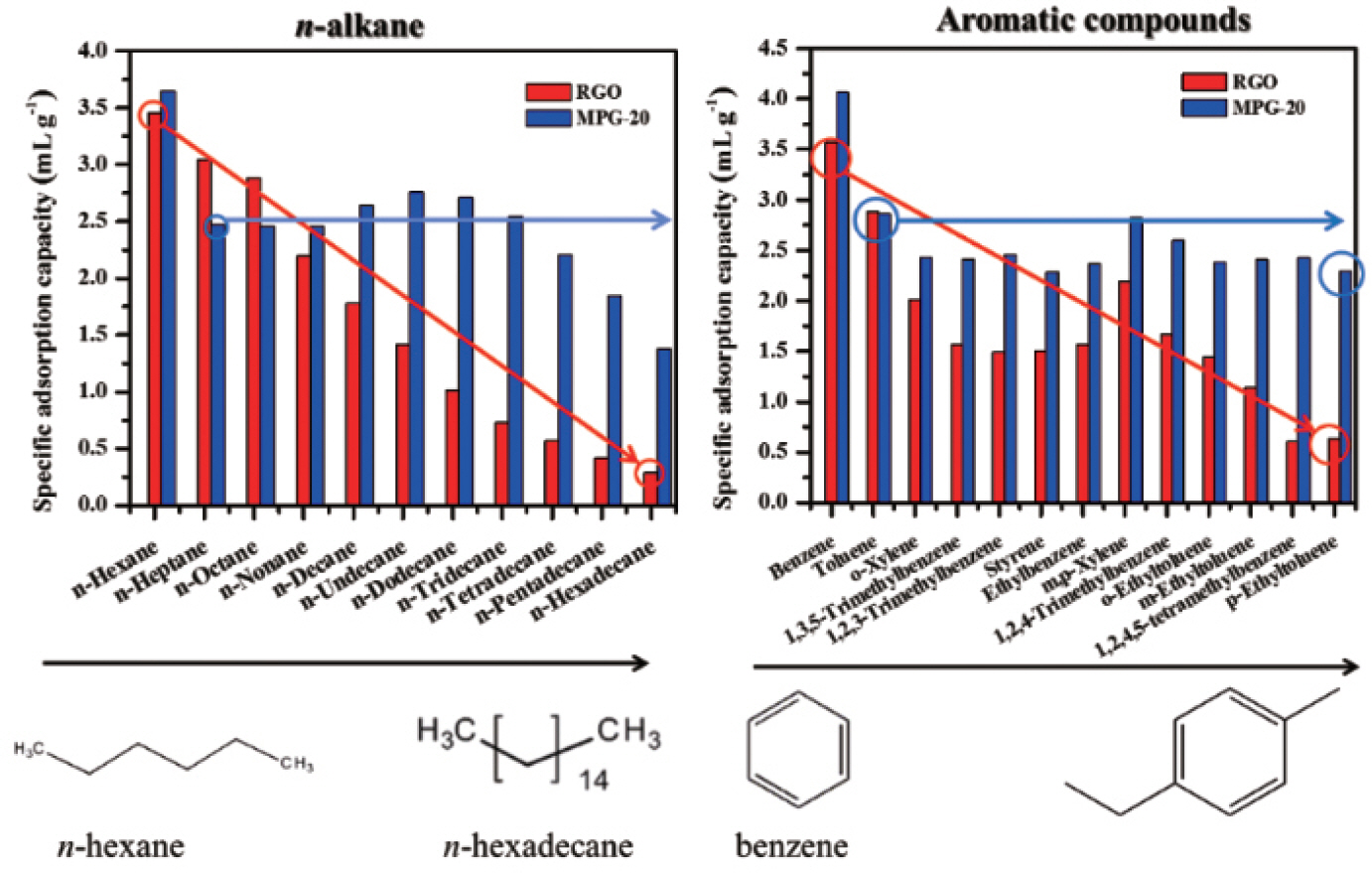
VOCs 흡착에 있어 흡착제의 기공 크기의 중요성은 서로 다른 기공 구조를 갖는 RGO와 MG 흡착제를 기준 농도 100 μg/ml (Supelco)의 크기가 다양한 총 52가지 실내 오염물질을 이용한 VOCs 흡착 테스트 결과를 통해 확인할 수 있다(Fig. 7). 소수성의 비교적 분자 크기가 큰 대기오염물질들은MG분체와 π-π 상호작용을 통해 VOCs 흡착 용량이 증가할 수 있으며, 특히 BTX(benzene, toluene, xylene)와 같은 방향족 탄화수소와 강한 흡착 거동을 나타낸다.
결과적으로 MG 분체는 RGO분체에 비해 많게는 40배까지 흡착 용량이 증가하였다. 흡착 용량은 작은 분자들의 경우 큰 차이가 없지만, 비교적 큰 분자들(n-hexadecane, p-ethyltoluene, D-limonene, 1,2,4,5-tetramethyl benzene 등)에서는 크게 차이가 난다. 이러한 차이는 RGO(비표면적 135 m2/g, 기공 크기 3.9 nm)에 비해 MG 의 상대적으로 넓은 비표면적(746 m2/g)과 기공 크기(9.5 nm)에서 기인하는 모양 및 크기 선택성 영향으로 설명할 수 있다.21)
또한 메조 다공성 그래핀의 표면을 카바모일 산화 포스핀(CMPO)으로 개질하여 희토류 원소를 흡착한 연구도 보고된 바 있다(Fig. 8).22) 희토류 원소는 촉매, 자석 및 디스플레이 응용을 포함한 다양한 하이테크 산업에서 주로 사용된다. 희토류 원소와 관련된 산업의 급속한 발전으로 희토류 원소가 자연계로 방출되어 암과 같은 호흡기 문제, 치아 손실과 같은 악영향을 유발한다. 따라서, 희토류 원소를 분리, 제거하기 위해 제올라이트, 금속 유기 골 격(metal organic frameworks, MOFs) 및 탄소 기반 물질과 같은 다양한 흡착 물질들이 활발히 연구되고 있다.
그중 메조 다공성 그래핀은 열린 기공 구조, 높은 비표면적으로 인하여 희토류 원소를 제거하기 위한 흡착제로 사용이 가능하다. 또한 메조 다공성 그래핀은 희토류 원소에 대한 높은 선택성을 갖는 적절한 작용기를 도입하는 것이 용이하다. 희토류 원소에 효과적인 흡착제로 질소가 도핑된 메조 다공성 그래핀(AMG) 표면에 카바모일 산화 포스핀(carbamoyl phosphine oxide moiety, CMPO)을 도입한 기능성 다공성 그래핀(CMPO-AMG) 흡착제가 보고되었다. CMPO 유도체는 굳은-무른 산염기 이론(hard-soft acid base theory)에 따라 희토류 원소와 안정한 육각 고리를 이루어 친화력이 강한 킬레이트 리간드로 알려져 있다. AMG의 아민기와 CMPO의 트리 에틸 포스포노 아세테이트의 에스터기 사이에 아마이드 결합을 통해 선택성이 높은 흡착체가 형성된다. 얻어진 CMPO-AMG의 희토류 원소에 대한 흡착 성능은 란타넘 이온(La3+)을 이용하여 평가되었다.23,24)
3-3. 나노 다공성 그래핀 기반 슈퍼커패시터
화석연료의 한계성과 에너지 문제가 지속적으로 대두 되면서, 효율적인 에너지 사용과 기후변화 대응을 위한 고성능의 에너지 저장 장치의 중요성이 점차 증가하고 있다. 슈퍼커패시터는 1853년 전기 이중층 모델이 처음으로 제안되었지만, 100년이 지나서야 비표면적이 넓은 활성탄이 등장하면서 상용화가 가능해졌다. 이후 메모리 백업용으로 주로 사용되었으며, 반영구적인 수명과 고출력 특성으로 최근 각종 전자 기기 및 신재생에너지 분야에서 수요와 관심이 지속적으로 증가하고 있다. 슈퍼커패시터의 에너지 밀도는 활물질의 커패시턴스와 셀 전압에 의해서 결정된다.
에너지밀도=1/2C cell E2
(에너지 밀도 단위: Wh/kg, 셀의 축전용량 C cell 단위: F/g, 셀의 전압 E 단위:V)
슈퍼커패시터는 사용되는 전극 활물질의 종류 및 저장메커니즘에 따라 크게 전기 이중층 커패시터(electrochemical double layer capacitor, EDLC)와 유사 커패시터(Pseudo-capacitor)로 나뉜다. 탄소 전극을 소재로 하는 EDLC는 이온과 활물질과의 물리적인 정전기적 흡·탈착에 의해 에너지를 저장하거나 공급한다. 리튬 이차 전지에 비해서 높은 출력과 무제한에 가까운 충·방전 수명, 친환경적 특성을 가져 차세대 에너지 저장 장치로 각광받고 있지만, 에너지 밀도(energy density)가 5~10 Wh/kg로 실제 적용에는 한계성을 지닌다. 반면, 유사 커패시터는 전극 활물질로서 금속 산화물 혹은 수산화물을 이용하여 표면 산화, 환원 반응에 의해서 상대적으로 EDLC보다 높은 에너지 밀도를 발현할 수 있다.
슈퍼커패시터는 빠른 충·방전 속도와 긴 사이클 수명, 높은 전력 밀도 등의 특성을 나타내야 한다. 전극 표면과 전해질의 계면 사이의 나노미터 수준 범위의 전하 분리를 통해 에너지를 빠르고 가역적으로 저장할 수 있어야 한다. 따라서, 전기 전도성과 비표면적이 커패시터의 성능을 결정하는 주요 요인이다. 다양한 탄소 기반 소재 중 그래핀은 넓은 비표면적과 우수한 전기 전도성을 가지고 있어 전극 물질 소재로 활발히 연구되고 있다.
이때 3차원 다공성 구조는 비표면적 증가와 적절한 크기의 기공이 3차원적으로 서로 잘 연결되어 전해질 이온의 원활한 이동을 촉진시킬 수 있다. 즉, 전극의 표면에 전해질이 쉽게 접근할 수 있어서 전기화학적 성능이 향상될 수 있다. 따라서 3차원 다공성 그래핀의 기공 특성 제어와 더불어 이종 원소 도핑을 통한 전도성 향상은 우수한 성능의 커패시터를 만드는 데 중요한 전략이 될 수 있다. 특히 붕소가 도핑된 메조 다공성 그래핀(Boron-doped mesoporous graphene, BMG)은 수열합성법으로 간단하게 합성될 수 있으며, 붕소의 화학적 배치(configuration)에 따라 전도성과 표면적이 달라진다. 붕소의 화학적 배치가 다른 BMG에 대한 물리화학적, 전기화학적 특성들을 비교한 연구가 진행된 바 있다. 결과적으로, 소성 과정을 거친 BMG(BMG-c, 1102 m2/g)는 수열합성법으로 얻어진 BMG(BMG-h, 997 m2/g)에 비해 상대적으로 넓은 비표면적을 나타냈다.25,26)
소성 과정 동안 BMG의 붕소와 산소의 함량, 붕소의 결합 배치(bonding configuration)가 바뀌어 미세기공의 증가에 따른 비표면적의 증가와 전기 전도성 등 전기화학적 특성에 영향을 준다. 소성 과정을 통해 비표면적이 증가한 BMG-c는 graphitic domain의 증가로 인해 EDLC 기여도가 증가하는 반면 이종 원소의 증발로 인해 붕소와 산소의 양이 감소하고, 붕소의 배치도 변화하여 유사 커패시터 기여도는 감소한다. BMG-c의 주된 붕소 결합 배치인 BC2 O는 슈퍼커패시터의 반응속도(kinetic) 성능 향상을 보여주는데, 그 이유는 전해질의 낮은 확산 저항(diffusion resistance)과 높은 전기 전도도 때문이다. 한편, 산소와 붕소의 함량이 상대적으로 높은 BMG-h의 주된 붕소 결합 배치인 BCO2는 사이클 안정성이 높으며 패러데이 산화 환원 반응(Faradic redox reaction)을 나타내기 때문에 낮은 전력 밀도에서 높은 전기용량을 보인다.
전극과 전해질 계면에서의 전하 이동(charge transfer)의 반응속도와 메커니즘을 살펴보기 위해 EIS (electrochemical impedance spectroscopy)를 측정한 결과, BMG-c와 비교했을 때 BMG-h는 상대적으로 산소 함량이 많고 반응속도가 느려 전도도가 낮아지므로 높은 진동수에서 더 큰 반원을 보인다. 전해질 저항(R s)은 BMG-c와 BMG-h가 표면 특성이 유사하여 거의 비슷한 값을 나타냈다. 반면, 전하 이동 저항(R ct)는 도핑과 열처리를 통해 낮아지는 것을 확인할 수 있다(MG: 0.17 Ω, BMG-h: 0.11 Ω, BMG-c: 0.08 Ω). 특히 BMG-c의 감소한 R ct는 높은 전기 전도도 결과와 일치하며, 이는 유사 커패시터의 기여도가 감소했음을 의미한다. BMG-h 는 이온의 확산 저항이 높았으며 전하의 저장 메커니즘은 주로 산화 환원에 의해 두드러지게 나타난다. BMG-c는 비표면적이 상대적으로 넓고 이온의 확산 저항이 낮아 EDLC 양상이 두드러진다. 이처럼 이종 원소 도핑을 통해 그래핀의 전기적 특성을 조절하여 슈퍼커패시터 성능을 향상시킬 수 있음을 확인할 수 있다.
3-4. 나노 다공성 그래핀 복합체 광촉매
광촉매는 입사하는 광자의 에너지가 광촉매의 띠 간격(band gap)과 같거나 클 때 그 빛을 흡수하여, 전자가 반도체의 원자가 띠(valence band)로부터 전도띠(conduction band)로 들뜬다. 반응물의 포텐셜 에너지(potential energy)가 반도체의 전도띠의 가장 낮은 포텐셜 에너지보다 높으면 들뜬 전자는 광촉매의 표면에서 반응물과 전기화학적 환원 반응을 할 수 있는데, 예를 들어 H+를 환원하여 H2로, 산소를 환원하여 O2- 라디칼로 바꾸거나, 또는 CO2를 환원시킬 수 있다. 반면, 반도체의 원자가 띠에서는, 들뜬 전자가 있었던 자리에 정공(hole)이 남는다. 이 정공의 가장 높은 포텐셜 에너지가 반응물의 포텐셜 에너지보다 높다면 전기화학적 산화 반응을 할 수 있다. 그러나 이 과정에서 반응에 참여하지 않은 들떴던 전자는 원자가 띠에 남은 정공에 재결합(recombination)하여 주로 빛 또는 열의 형태로 에너지를 방출한다.27,28,29)
전자와 정공이 재결합하면 광촉매 활성을 나타내지 않으므로, 이러한 재결합을 막는 것이 광촉매 반응의 효율을 높일 수 있다. 따라서 전자와 정공을 성공적으로 분리하여 재결합을 막기 위해, 특히 전도성이 우수한 그래핀 기반 물질을 도입하는 것이 주요한 전략 중 하나이다. 전자 전달이 용이한 그래핀의 구조 때문에 반도체의 전도띠로 들뜬 전자는 그래핀으로 쉽게 전달되어 다시 반도체의 원자가 띠로 돌아가는 것을 막을 수 있다. 다양한 전이 금속 산화물 반도체와 그래핀의 복합체들 중에서, 이산화 타이타늄(TiO2)과 그래핀 복합체는 광촉매의 효율 및 전기화학적 특성을 향상시킬 수 있어 주목받고 있다.30)
반도체 소재를 이용한 촉매 반응으로 유기 오염물질을 분해하는 것은 폐수 처리 산업에서 효과적인 기술로써 많은 관심을 받기 시작했다. 특히 TiO2는 저렴하고 자연에 풍부하게 존재하며, 고온에서도 구조적 안정성을 유지하는 등 여러 장점을 가져 오랜 기간 관련 연구가 진행되었다. 그러나 TiO2는 광 유도된 전자와 정공 쌍이 빠르게 재결합하기 때문에 양자 효율이 낮고, 띠 간격이 넓어(3.2 eV) 태양 빛(약 3~5% UV 광을 포함)을 광원으로 활용하는데 제한이 있다. 따라서 이종 원소를 도핑하여 반도체의 띠 간격을 조절하거나, 그래핀을 전자 받개로 사용하여 전자-정공 쌍의 재결합을 제어하여 촉매 효율을 증대시킬 수 있다.31)
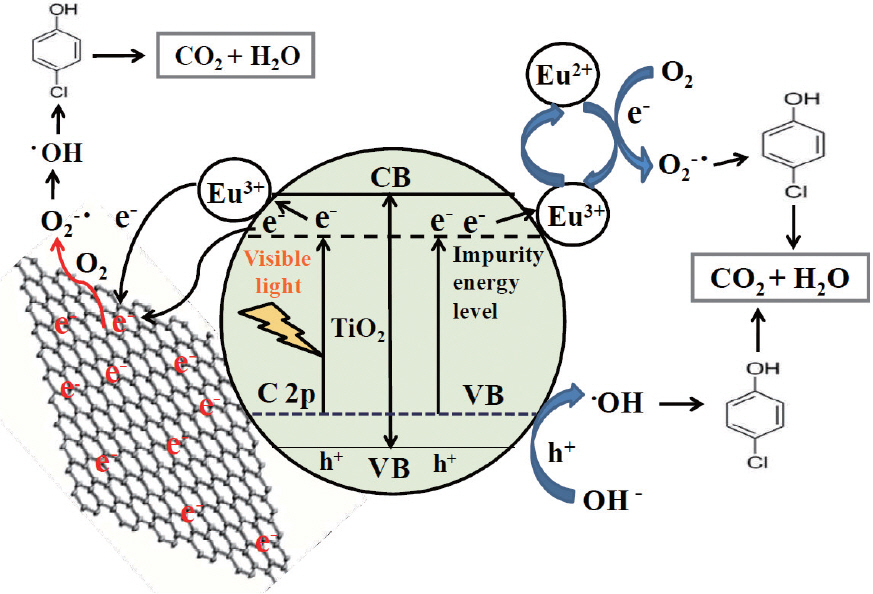
유로퓸 이온(Eu3+)이 도핑된 TiO2는 띠 간격 조절을 통해 가시광선에 감응하는 광촉매로 응용될 수 있는데, 이때 메조 다공성 그래핀 구조를 적용하여 전자-정공 쌍 재결합을 제어할 수 있을 뿐만 아니라 비표면적과 기공의 부피를 증가 시켜 광촉매 활성을 향상시킬 수 있다. 또한, 그래핀의 층상형 구조는 anatase TiO2 결정 성장 자리로써 작용하며 TiO2 나노입자 간의 응집 현상을 막아준다. TiO2에서 광 유도 된 전자는 계면을 통해 쉽게 그래핀으로 이동할 수 있어 전하 이동 효율이 증가한다. 결과적으로, 가시광선 조건의 광원(tungsten halogen vapour lamp, λ > 410 nm)에 240분간 노출시킨 후 4-cholorophenol의 분해의 정도를 비교하였을 때, 초기 농도의 약 88.6 %를 감소시켜 기존의 Eu2 O3/TiO2 복합체(~55%)에 비해 향상된 광 효율을 확인할 수 있다.32)
4. 결론
나노기술은 10억분의 1 m인 1 nm 수준에서 원자나 분자 구조 등을 제어함으로써 기존 소재에서는 보지 못했던 새로운 현상을 이해하고 응용한다. 그 특성을 응용해 에너지 전환 및 저장 장치, 흡착제, 촉매 등 전 산업 분야에서 이용되고 있다. 특히 그래핀은 탄소의 sp2 혼성 평면 구조에서 오는 독특한 성질 덕분에 다양한 분야에서 응용이 가능하다. 그래핀의 자기응집 현상에 의해 비표면적이 감소하는 단점은 3차원 다공성 구조를 형성함으로써 극복될 수 있으며 이러한 물질은 더 다양한 분야에서 응용성이 증대될 수 있다.
여러 종류의 탄소 물질이 0차원에서 시작하여 1차원, 2 차원, 그리고 3차원 등 다양하게 연구되고 있다. 각각의 물질들이 가지고 있는 장점을 특징으로 하여 목적에 적합한 기능성 탄소 소재를 합성할 수 있다. 삼차원 구조의 나노 다공성 그래핀은 다양한 마이셀 주형을 이용하여 기공 크기를 조절할 수 있으며, 본론에서 다룬 바와 같이 GO 층 사이의 화학 결합을 조절하여 기공 특성을 제어하는 메커니즘에 대한 이해를 바탕으로 연구목적에 최적화된 다공성 물질을 합성할 수 있다.
기공 특성이 조절된 나노 다공성 그래핀은 특정 화학종의 선택적인 흡착 및 담지에 용이하며 증대된 비표면적과 기공 부피로 인해 전기적, 자기적, 광학적 성능을 향상시킬 수 있어 앞으로도 신소재 연구 발전에 큰 기여를 할 소재로 기대된다. 미래에 한정된 자원을 활용하기 위해서는 보다 진보된 기술과 신소재가 필요하며, 국가 경쟁력 확보에 기여할 수 있는 기술 개발의 시작은 소재로부터 출발한다. 소재에 대한 이해와 응용은 더 발전된 기술 개발로 이끌어줄 수 있다.
References
Biography

◉◉정 현
◉2003년 서울대학교 화학과 박사
◉2004-2005년 ICMCB-CNRS 박사후 연구원
◉2007년-현재 동국대학교 이과대학 화학과 교수

◉◉강 예 인
◉2018년 동국대학교 화학과 학사
◉2019년-현재 동국대학교 화학과 석사과정