2.1 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņ£äĒĢ£ SPS
ņĀäĻ│Āņāü ņĀäņ¦ĆņŚÉņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņżæņÜöĒĢ£ ņåīņ×¼ ņżæņŚÉ ĒĢśļéśņØ┤ļ®░, ņØ╝ļ░śņĀüņ£╝ļĪ£ ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀüņÜ®ņØä ņ£äĒĢ┤ņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ĒŖ╣ņä▒ņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņĪ░Ļ▒┤ņØä ņČ®ņĪ▒ĒĢ┤ņĢ╝ ĒĢ£ļŗż.
17)
(1) ņāüņś©ņŚÉņä£ 10ŌłÆ4 S cmŌłÆ1 ļ│┤ļŗż ļåÆņØĆ ņØ┤ņś© ņĀäļÅäļÅä
(2) ļ”¼ĒŖ¼ ĻĖłņåŹĻ│╝ ņé░ĒÖö/ĒÖśņøÉ ļ░śņØæņŚÉ ļö░ļźĖ ņĢłņĀĢņä▒
(3) ļåÆņØĆ ņåīĻ▓░ ĒŖ╣ņä▒
(4) ņĀäĻĘ╣Ļ│╝ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł Ļ│äļ®┤ņŚÉņä£ ļé«ņØĆ ņĀæņ┤ē ņĀĆĒĢŁ
(5) ļåÆņØĆ ņåīĻ▓░ ņś©ļÅäņŚÉ ļö░ļźĖ ĻĄ¼ņĪ░ņĀü ņĢłņĀĢņä▒
(6) ļåÆņØĆ ĻĖ░Ļ│äņĀü Ļ░ĢļÅä
ņĄ£ĻĘ╝ ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤ ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀüņÜ®ņØä ņ£äĒĢ£ Garnet, NASiCON, Perovskite ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņĀ£ņĪ░ļÉśņ¢┤ Ļ│ĄņĀĢ ļÅÖņĢłņŚÉ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö Ļ▓░ņĀĢļ”ĮĻ│╝ Ļ▓░ņĀĢļ”ĮĻ│äņØś ņĀ£ņ¢┤ļź╝ ĒåĄĒĢ┤ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļź╝ Ē¢źņāüņŗ£Ēé¼ ņłś ņ׳ņŚłļŗż.
Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ Li
5 La
3 M
2 O
12 (M=Nb, Ta, Bi) ĒÖöĒĢÖņĀü ĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦Ćļ®░, ļ”¼ĒŖ¼ ĻĖłņåŹņŚÉ ļīĆĒĢ£ ĒÖöĒĢÖņĀü ļ░Å ņŚ┤ņĀü ņĢłņĀäņä▒Ļ│╝ ĒÖśĻ▓Į ņ╣£ĒÖöņä▒ ļō▒ņØś ņÜ░ņłśĒĢ£ ĒŖ╣ņä▒ņ£╝ļĪ£ ļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ░Ć ņ¦äĒ¢ēļÉśņŚłļŗż.
18) ĻĘĖļ¤¼ļéś Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ĻĖ░ņĪ┤ņØś Ļ│Āņāü ĒĢ®ņä▒ļ▓ĢņØä ĒåĄĒĢ┤ ņøÉĒĢśĻ│Āņ×É ĒĢśļŖö cubic ņāüņØä Ļ░Ćņ¦ĆļŖö Li
7 La
3 Zr
2 O
12 (LLZO)ņØä ĒĢ®ņä▒ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ļåÆņØĆ ņåīĻ▓░ ņś©ļÅä (> 1230 ┬░C) ļ░Å ĻĖ┤ ņåīĻ▓░ ņŗ£Ļ░ä (> 30ŌĆō40 h)ņØä ĒĢäņÜöļĪ£ ĒĢ£ļŗż. ņØ┤ļ¤░ cubic ņāüļź╝ Ļ░Ćņ¦ĆļŖö Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ tetragonal ņāüņØä Ļ░Ćņ¦ĆļŖö Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł(10
ŌłÆ6 S cm
ŌłÆ1) ļ│┤ļŗż ņāüņś©ņŚÉņä£ ļåÆņØĆ 10
ŌłÆ3 S cm
ŌłÆ1ņØś ļ▓īĒü¼ ņØ┤ņś© ņĀäļÅäļÅäļź╝ Ļ░Ćņ¦äļŗż. ĻĘĖļ¤¼ļéś ļåÆņØĆ ņś©ļÅä ļ░Å ĻĖ┤ ņŗ£Ļ░äņØä ĒĢäņÜöļĪ£ ĒĢśļŖö ĻĖ░ņĪ┤ņØś ĒĢ®ņä▒ļ▓ĢņØĆ LLZO ĻĄ¼ņĪ░ņŚÉņä£ LiņØ┤ ļ╣ĀņĀĖļéśņśżĻ▒░ļéś ņ”Øļ░£ļĪ£ ņØĖĒĢ┤ ņøÉĒĢśņ¦Ć ņĢŖņØĆ La
2 Zr
2 O
7ņØś ļČłņł£ļ¼╝ ņāüņØä ĒśĢņä▒ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļź╝ ņĀĆĒĢśņŗ£Ēé©ļŗż. ļśÉĒĢ£, ĻĖ░ņĪ┤ņØś ļ░®ļ▓Ģņ£╝ļĪ£ ņåīĻ▓░ļÉ£ LLZO Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņØ╝ļ░śņĀüņ£╝ļĪ£ ļé«ņØĆ ļ░ĆļÅäņŚÉ ļö░ļźĖ Ļ│äļ®┤ ņĀĆĒĢŁņØś ņ”ØĻ░ĆļĪ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć ļé«ņĢäņ¦äļŗż. ņØ┤ļ¤░ ņĖĪļ®┤ņŚÉņä£ SPS Ļ│ĄņĀĢņØĆ ļé«ņØĆ ņåīĻ▓░ ņś©ļÅä ļ░Å ņ¦¦ņØĆ ņåīĻ▓░ ņŗ£Ļ░äņØä ņĀ£Ļ│ĄĒĢśņŚ¼ ļ░öļ×īņ¦üĒĢ£ ĻĄ¼ņĪ░ ĒśĢņä▒ņØä ņ£äĒĢ┤ Ļ│ĄņĀĢ ņĪ░Ļ▒┤ņØä ņēĮĻ▓ī ņĀ£ņ¢┤ĒĢśĻ│Ā, ņØ┤ļĪĀ ļ░ĆļÅäņŚÉ ĻĘ╝ņĀæĒĢ£ ļ░ĆļÅäļź╝ Ļ░Ćņ¦ĆļŖö Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ĒĢ®ņä▒ĒĢĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ĻĖ░ņĪ┤ņØś ĒĢ®ņä▒ Ļ│ĄņĀĢ ļ│┤ļŗż Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ĒĢ®ņä▒ĒĢśļŖöļŹ░ ņĀüĒĢ®ĒĢ£ Ļ│ĄņĀĢņ£╝ļĪ£ ļ¦ÄņØĆ Ļ┤Ćņŗ¼ņØä ļ░øĻ│Ā ņ׳ļŗż.
ĻĘĖņŚÉ ļö░ļØ╝, Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ĒĢ®ņä▒ĒĢśļŖöļŹ░ SPS Ļ│ĄņĀĢņØä ņØ┤ņÜ®ĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ Ēśäņ×¼ ļ¦ÄņØ┤ ņ¦äĒ¢ē ņżæņŚÉ ņ׳ļŗż. 2014ļģäļÅäņŚÉ Zhang ĻĘĖļŻ╣ņŚÉņä£ļŖö AlņØ┤ ņ╣śĒÖśļÉ£ cubic ņāüņØä Ļ░Ćņ¦ĆļŖö LLZOļź╝ SPSļź╝ ĒåĄĒĢ┤ 1150 ┬░C ņåīĻ▓░ ņś©ļÅäņŚÉņä£ 10ļČä ņØ┤ļé┤ļĪ£ ņĀ£ņ×æĒĢśņśĆļŗż. ņØ┤ļĀćĻ▓ī ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ 99.8% ļåÆņØĆ ņāüļīĆļ░ĆļÅäņÖĆ ņāüņś©ņŚÉņä£ 5.7 ├Ś 10
ŌłÆ4 S cm
ŌłÆ1ņØś ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļāłļŗż.
19) ņØ┤ ņŚ░ĻĄ¼ļŖö ĻĖ░ņĪ┤ ņŚ░ĻĄ¼ņŚÉņä£ cubic ņāüņØä Ļ░Ćņ¦ĆļŖö LLZOļź╝ ĒĢ®ņä▒ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ĒĢäņÜöļĪ£ ĒĢśļŖö ņś©ļÅäĻ░Ć ĻĖ░ņĪ┤ņØś Ļ│Āņāü ļ░śņØæ ĒĢ®ņä▒(1250 ┬░C) ļ│┤ļŗż ņāüļīĆņĀüņ£╝ļĪ£ ļé«ņØĆ Ļ▓āņØä ļ│┤ņŚ¼ņŻ╝ņŚłņ£╝ļ®░, ņ£ä ņŚ░ĻĄ¼ņŚÉņä£ ļŹö ņżæņÜöĒĢ£ ņé¼ĒĢŁņØĆ ņ¦¦ņØĆ ņåīĻ▓░ ņŗ£Ļ░äņ£╝ļĪ£ ņØĖĒĢ┤ LiņØś ņ”Øļ░£ņØä ļ¦ēņĢä ĒĢ®ņä▒ ņŗ£ ņČöĻ░ĆņĀüņØĖ Li resourceņØś ņČöĻ░ĆĻ░Ć ĒĢäņÜöĒĢśņ¦Ć ņĢŖļŖö ļŗżļŖö Ļ▓āņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ļŗżļźĖ ņŚ░ĻĄ¼ļĪ£ ļČäļ¼┤ ņŖżĒöäļĀłņØ┤ ņŚ┤ļČäĒĢ┤ ļ▓Ģ (nebulized spray pyrolysis)ņØä Ļ░Ćņ¦ĆĻ│Ā ĒĢ®ņä▒ļÉ£ 0.3Ōł╝5 ╬╝mņØś Ēü¼ĻĖ░ļź╝ Ļ░Ćņ¦ĆļŖö Li
7-3x La
3 Zr
2 Al
z O
12 (x= 0.15, 0.17, 0.20) ļČäļ¦ÉņØä ĒĢ®ņä▒ Ēøä 950 ┬░C ņŚÉņä£ 10ļČä ļÅÖņĢł SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņ×æĒ¢łļŗż.
20) XRDļź╝ ņØ┤ņÜ® ĻĄ¼ņĪ░ ļČäņäØ Ļ▓░Ļ│╝, AlņØ┤ ļÅäĒĢæ ņä▒ļČäņŚÉ Ļ┤ĆĻ│äņŚåņØ┤ ņåīĻ▓░ļÉ£ ļ¬©ļōĀ ņŗ£ļŻīņŚÉņä£ La
2 ZrO
7Ļ│╝ tetragonal ņāü LLZOņØä ĒĢ©ņ£ĀĒĢśĻ│Ā ņ׳ļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. ņØ┤ Ļ▓░Ļ│╝ļŖö Zhang ĻĘĖļŻ╣ņØś ņŚ░ĻĄ¼ņŚÉņä£ ļ╣äņŖĘĒĢ£ ņś©ļÅä(900ŌĆō1000 ┬░C)ņŚÉņä£ ņåīĻ▓░ļÉ£ AlņØ┤ ņ╣śĒÖśļÉ£ LLZOņŚÉņä£ ļæÉĻ░£ņØś ļČłņł£ļ¼╝ ņāüņØ┤ ļ░£Ļ▓¼ļÉśņ¢┤ ļ╣äņŖĘĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆņ£╝ļ®░, ņåīĻ▓░ ņś©ļÅäņŚÉ ļö░ļØ╝ La
2 ZrO
7Ļ│╝ tetragonal ņāüņØä Ļ░Ćņ¦ĆļŖö LLZOĻ░Ć ņāØņä▒ļÉśļŖö ļåÆņØĆ ļ»╝Ļ░ÉĒĢ©ņØä ļéśĒāĆļāłļŗż. ĻĘĖļ¤¼ļéś ņØ┤Ļ▓░Ļ│╝ļŖö ļæÉĻ░£ņØś ļČłņł£ļ¼╝ ņāü ĒśĢņä▒ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņāüņś©ņŚÉņä£ ļåÆņØĆ ņØ┤ņś© ņĀäļÅäļÅäņØĖ 3 ├Ś 10
ŌłÆ4 S cm
ŌłÆ1 ļ░Å 0.38 eVņØś ĒÖ£ņä▒ĒÖö ņŚÉļäłņ¦Ćļź╝ ļéśĒāĆļāłņ£╝ļ®░, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļŖö cubic ņāüņØä Ļ░Ćņ¦ĆļŖö LLZOņØś ņØ┤ņś© ņĀäļÅäļÅäņÖĆ ļ╣äņŖĘĒĢ£ Ļ░ÆņØĆ ļéśĒāĆļāłļŗż. ņØ┤ Ļ▓░Ļ│╝ļŖö tetragonal ņāüņØä Ļ░Ćņ¦ĆļŖö LLZOļŖö SPS Ļ│ĄņĀĢ ļÅÖņĢł ļ»ĖņäĖ ļ│ĆĒśĢņØś ļÅäņ×ģņŚÉ ņØśĒĢ┤ ņĢ╝ĻĖ░ļÉśņŚłņØä Ļ▓āņØ┤ļØ╝ ņśłņāüĒ¢łņ£╝ļ®░, tetragonal ņāüņØä Ļ░Ćņ¦ĆļŖö LLZO ņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ Li ņØ┤ņś© ņĀäļÅäļÅäņŚÉ ņśüĒ¢źņØä ņŻ╝ņ¦Ć ņĢŖļŖöļŗżĻ│Ā ņäżļ¬ģĒ¢łļŗż. ļśÉĒĢ£, Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ LiĻ│╝ ļ░śņØæņä▒ ĒÖĢņØĖņØä ņ£äĒĢ┤ņä£ Li|Li
3x La
3 Zr
2 Al
z O
12|Li ņģĆņØä ĻĄ¼ņä▒ 100 h ļÅÖņĢł ņé¼ņØ┤Ēü┤ ĒŖ╣ņä▒ņØä ĒÅēĻ░ĆĒĢ£ Ļ▓░Ļ│╝ ņä▒ļŖź ņĀĆĒĢś ņŚåņØ┤ ņÜ░ņłśĒĢ£ ņé¼ņØ┤Ēü┤ ĒŖ╣ņä▒ņØä ļ│┤ņśĆņ£╝ļ®░, ņé¼ņØ┤Ēü┤ Ēøä Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łĻ│╝ LiĻ│╝ņØś Ļ│äļ®┤ ņĀĆĒĢŁ ņ”ØĻ░ĆĻ░Ć ņŚåļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż.
21) ņ£äņŚÉ ļæÉ ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļź╝ ļ░öĒāĢņ£╝ļĪ£ SPS Ļ│ĄņĀĢņØĆ ļåÆņØĆ ļ░ĆļÅä ļ░Å ņØ┤ņś© ņĀäļÅäļÅäļź╝ Ļ░Ćņ¦ĆļŖö LLZO Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ļ╣ĀļźĖ ņåīĻ▓░ņØä ĒåĄĒĢ┤ņä£ ņĀ£ņ×æĒĢĀ ņłś ņ׳ļŗżļŖö Ļ▓āņØä ĒÖĢņØĖņŗ£ņ╝£ņŻ╝ņŚłņ£╝ļ®░, SPSņØś ņåīĻ▓░ ņś©ļÅäĻ░Ć ĻĖ░ņĪ┤ņØś ņåīĻ▓░ ļ░®ļ▓Ģļ│┤ļŗż ļé«ļŹöļØ╝ļÅä SPS Ļ│ĄņĀĢ ņŗ£ ņś©ļÅäļŖö ļČäļ¦É Ēæ£ļ®┤ņŚÉņä£ ļ░£ņāØĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņČöņĖĪļÉśļŖö ļČłĒĢäņÜöĒĢ£ ļČłņł£ļ¼╝ ņāü ĒśĢņä▒ņØä ņĄ£ņåīĒÖöĒĢśĻĖ░ ņ£äĒĢ┤ņä£ SPS Ļ│ĄņĀĢ ņĄ£ņĀüĒÖöļź╝ ņ£äĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ļŹö ĒĢäņÜöĒĢśļŗżĻ│Ā ņĀ£ņĢłĒ¢łļŗż.
ņĄ£ĻĘ╝ņŚÉļŖö Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļź╝ ņ”ØĻ░Ćņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ņä£ Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņŚÉ ņ¢æņØ┤ņś© ļÅäĒĢæņØä ĒåĄĒĢ┤ ĻĄ¼ņĪ░ ņĢłņĀĢņä▒ ļ░Å ņØ┤ņś© ņĀäļÅäļÅäļź╝ Ē¢źņāüņŗ£Ēé¼ ņłś ņ׳ņŚłņ£╝ļ®░, SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļŹöņÜ▒ ļåÆņØ╝ ņłś ņ׳ņŚłļŗż. Baek ĻĘĖļŻ╣ņØĆ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ĻĄ¼ņĪ░ņĀü ņĢłņĀĢņä▒ņØä Ē¢źņāüņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ņä£ LLZOņŚÉ TaĻ░Ć ļÅäĒĢæļÉ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-d Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ĒĢ®ņä▒Ē¢łņ£╝ļ®░,
22) SPS Ļ│Ąļ▓Ģņ£╝ļĪ£ ņĀ£ņ×æļÉ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-dņØś ļ»ĖņäĖ ĻĄ¼ņĪ░ņÖĆ ņØ┤ņś© ņĀäļÅäļÅäņŚÉ ļīĆĒĢ£ ĒŖ╣ņä▒ņØä ĻĖ░ņĪ┤ņØś ņåīĻ▓░ Ļ│Ąļ▓ĢĻ│╝ ļ╣äĻĄÉ ļČäņäØĒĢśņśĆļŗż. (
Fig. 3) ĻĖ░ņĪ┤ņØś ņĀäĒśĢņĀüņØĖ Ļ│ĄņĀĢņ£╝ļĪ£ ņåīĻ▓░ĒĢ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-dļŖö ĻĖ░Ļ│Ą ĒśĢņä▒ņŚÉ ļö░ļźĖ ļåÆņØĆ Ļ▓░ņĀĢ ņ×ģĻ│ä ņĀĆĒĢŁņØä ņ£ĀļÅäĒĢśļŖö ņĀäņ▓┤ ĻĄ¼ņĪ░ņŚÉ Ļ▒Ėņ│É ļČłĻĘĀņØ╝ĒĢ£ ļ░ĆļÅäļź╝ ļ│┤ņśĆņ£╝ļ®░(
Fig. 3a), ņØ┤ņÖĆ ļ░śļīĆļĪ£ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņåīĻ▓░ļÉ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-dļŖö Ļ│Āļ░ĆļÅä ĻĄ¼ņĪ░ļź╝ Ļ░ĆņĀĖ ņāüņś©ņŚÉņä£ ļåÆņØĆ ņØ┤ņś© ņĀäļÅäļÅäņØĖ 1.35 ├Ś 10
ŌłÆ3 S cm
ŌłÆ1ņØä ļéśĒāĆļāłļŗż. (
Fig. 3c) ņØ┤ Ļ▓░Ļ│╝ļŖö ļ»ĖņäĖĻĄ¼ņĪ░ Ļ▓░Ļ│╝ņŚÉņä£ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ĻĖ░ņĪ┤ņŚÉ ņĀäĒśĢņĀüņØĖ ņåīĻ▓░ņØä ĒåĄĒĢ┤ ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ĻĖ░Ļ│ĄņØ┤ ĒśĢņä▒ļÉ£ ļ░śļ®┤ņŚÉ, SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ĻĖ░Ļ│Ą ņŚåņØ┤ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ ņ╣śļ░ĆĒĢśĻ▓ī ĒśĢņä▒ļÉ£ Ļ▓āņŚÉ ĻĖ░ņØĖĒĢ£ļŗżĻ│Ā ĒīÉļŗ©Ē¢łļŗż. (
Fig. 3b)
Fig.┬Ā3.
Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-dņØś ļ»ĖņäĖĻĄ¼ņĪ░ ļ░Å ņØ┤ņś© ņĀäļÅäļÅä ĒŖ╣ņä▒. (a) ņĀäĒśĢņĀüņØĖ Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ 1230 ┬░CņÖĆ 1200 ┬░CņŚÉņä£ ņåīĻ▓░ļÉ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-d ņØś SEM. (b) SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ 700ŌĆō1000 ┬░CĻ╣īņ¦Ć ņåīĻ▓░ļÉ£ Li
7-xLa
3Zr
1.5Ta
0.5O
12-dņØś SEM. (c) ņĀäĒśĢņĀüņØĖ ņåīĻ▓░Ļ│╝ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņåīĻ▓░ļÉ£ Li
7-x La
3 Zr
1.5 Ta
0.5 O
12-dņØś ņØ┤ņś© ņĀäļÅäļÅä.
22)

LLZO ļ░Å Li
7 La
3 Ta
2 O
12 ņÖĖņŚÉļÅä, Li
5 La
3 Nb
2 O
12 ļ░Å Li
5 La
3 Bi
2 O
12ņÖĆ Ļ░ÖņØĆ ļŗżļźĖ ņóģļźśņØś Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ SPSņŚÉ ņØśĒĢ┤ ņĀ£ņĪ░ļÉśĻ│Ā, ņÜ░ņłśĒĢ£ ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļé┤ņŚłļŗż. Mohamad ĻĘĖļŻ╣ņØĆ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ Li
5 La
3 Nb
2 O
12 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņĪ░ĒĢśņśĆļŗż.
23) ņĀäĒśĢņĀüņØĖ Ļ│ĄņĀĢņ£╝ļĪ£ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņ×ģĻ│ä ņé¼ņØ┤ņ”łĻ░Ć 1ŌĆō2 ╬╝mņØś Ļ▒░ņ╣£ ĻĄ¼ņĪ░ļź╝ Ļ░¢ļŖö ļ░śļ®┤, SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ 50ŌĆō100 nmņØś Ēü¼ĻĖ░ļź╝ Ļ░¢ļŖö ļéśļģĖ Ēü¼ĻĖ░ņØś ņ×ģĻ│äļź╝ Ļ░¢ļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. ļ»ĖņäĖĻĄ¼ņĪ░ ļČäņäØ Ļ▓░Ļ│╝ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņŚÉņä£ļŖö ĻĖ░Ļ│ĄņØ┤ Ļ░ÉņåīĒĢśĻ│Ā ņ×ģĻ│ä Ļ░ä Ļ▓░ĒĢ©ņØ┤ Ļ░£ņäĀļÉ£ Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. ĻĘĖ Ļ▓░Ļ│╝, 850 ŌäāņŚÉņä£ SPSņŚÉ ņØśĒĢ┤ ņåīĻ▓░ ļÉ£ Li
5 La
3 Nb
2 O
12ļŖö ņāüņś©ņŚÉņä£ 3.7 ├Ś 10
ŌłÆ5 S cm
ŌłÆ1ņØś ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļāłņ£╝ļ®░, ņĀäĒśĢņĀüņØĖ Ļ│ĄņĀĢņ£╝ļĪ£ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅä ļ│┤ļŗż ļåÆņØĆ Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż.
24) ļśÉļŗżļźĖ Ļ▓░Ļ│╝ļĪ£, SPSņŚÉ ņØśĒĢ┤ ņĀ£ņĪ░ļÉ£ Li
5 La
3 Bi
2 O
12 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ Garnet ĻĖ░ļ░ś ĻĄ¼ņĪ░ ļ░Å 97% ņāüļīĆ ļ░ĆļÅä ļéśĒāĆļāłņ£╝ļ®░, Li
5 La
3 Bi
2 O
12 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļŖö ņāüņś©ņŚÉņä£ 5.1 ├Ś 10
ŌłÆ5 S cm
ŌłÆ1ņØś ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļāłļŗż.
25)
ļśÉļŗżļźĖ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łļĪ£ NASICON ĻĖ░ļ░ś LiM2(PO4)3 (M= Ti, Ge, Zr, Hf)ņØĆ Li ņØ┤ņś©ņŚÉ ņ£Āļ”¼ĒĢ£ ņĀäļÅä Ēä░ļäÉņØä Ļ░¢ļŖö ļśÉ ļŗżļźĖ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ĻĘĖļŻ╣ņØ┤ļ®░, ļīĆĻĖ░ņŚÉņä£ ļåÆņØĆ ĒÖöĒĢÖņĀü ņĢłņĀĢņä▒ņŚÉ ļĢīļ¼ĖņŚÉ ļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ░Ć ļÉśņ¢┤ņÖöļŗż. NASICON ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļŖö ņøÉņåī ņ╣śĒÖśņŚÉ ņØśĒĢ┤ Ē¢źņāüļÉśņŚłņ¦Ćļ¦ī, Garnet ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łĻ│╝ ņ£Āņé¼ĒĢśĻ▓ī ļåÆņØĆ Ļ▓░ņĀĢļ”ĮĻ│ä ņĀĆĒĢŁĻ│╝ ļåÆņØĆ ļ░ĆļÅäļź╝ Ļ░Ćņ¦ĆļŖö Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņ¢╗ļŖöļŹ░ ņ¢┤ļĀżņøĆņØ┤ ņ׳ņ¢┤ ņØ┤ļ¤░ ļ¼ĖņĀ£ļōżņØĆ NASICON ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ņāüņÜ®ĒÖöļź╝ ņĀ£ĒĢ£Ē¢łļŗż. ņĄ£ĻĘ╝ SPSļŖö ļåÆņØĆ Ļ│äļ®┤ ņĀĆĒĢŁņŚÉ ļīĆĒĢ£ ļ¼ĖņĀ£ļź╝ ĒĢ┤Ļ▓░ĒĢśĻ│Ā, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ļ░ĆļÅäļź╝ Ē¢źņāü ņŗ£ņ╝£ NASICON ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅä Ē¢źņāüņØä ņ£äĒĢ┤ ļ¦ÄņØ┤ ņĀüņÜ®ļÉśņ¢┤ņÖöļŗż.
Chang ĻĘĖļŻ╣ņØĆ LiTi
2(PO
4)
3 (LTP), Li
1.3 iAl
0.3 Ti
1.7(PO
4)
3 (LATP), and Li
1.3 Al
0.3 Ti
1.7(PO
4)
2.9(VO
4)
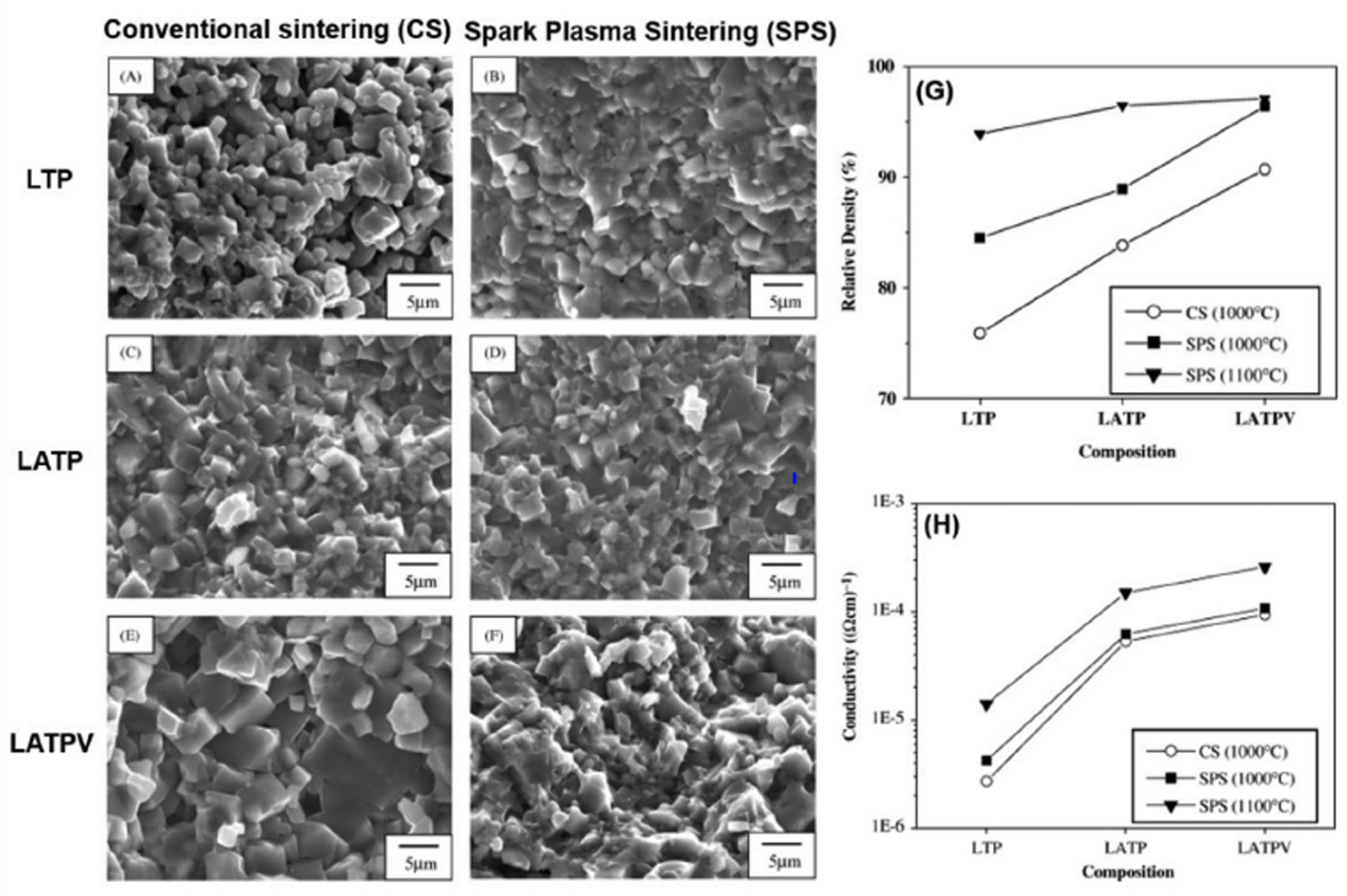
0.1 (LATPV) Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä SPSņÖĆ ņĀäĒśĢņĀüņØĖ ņåīĻ▓░ Ļ│ĄņĀĢņ£╝ļĪ£ ņĀ£ņĪ░ Ēøä ņåīĻ▓░ ļ░®ļ▓ĢĻ│╝ ņĪ░Ļ▒┤ņŚÉ ļö░ļØ╝ LTP, LATP ļ░Å LATPVņØś ļ»ĖņäĖ ĻĄ¼ņĪ░Ļ░Ć ņØ┤ņś© ņĀäļÅäļÅäņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ĒÅēĻ░ĆĒ¢łļŗż.
26) (
Fig. 4) ņĀäĒśĢņĀüņØĖ Ļ│Ąļ▓Ģņ£╝ļĪ£ ņåīĻ▓░ļÉ£ LTPļŖö 76%ņØś ņāüļīĆ ļ░ĆļÅäņŚÉ ļö░ļźĖ ļ»ĖņäĖ ĻĖ░Ļ│ĄņØä Ļ░Ćņ¦ĆļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łņ£╝ļ®░, ĻĘĖņÖĆ ļŗ¼ļ”¼ 1100 ŌäāņŚÉņä£ SPSņŚÉ ņØśĒĢ┤ ņåīĻ▓░ļÉ£ LTPļŖö ļ»ĖņäĖ ĻĖ░Ļ│Ą ņŚåļŖö 94%ņØś ņāüļīĆ ļ░ĆļÅäļź╝ Ļ░Ćņ¦ĆļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. (
Fig. 4g) ĻĘĖ Ļ▓░Ļ│╝, SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņĀ£ņ×æļÉ£ LAPĻ░Ć Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļŖö ĻĖ░ņĪ┤ņØś ņåīĻ▓░ Ļ│ĄņĀĢņ£╝ļĪ£ ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł(2.7 ├Ś 10
ŌłÆ5 S cm
ŌłÆ1) ļ│┤ļŗż ļåÆņØĆ ņāüņś©ņŚÉņä£ 1.4 ├Ś 10
ŌłÆ6ņØä ļéśĒāĆļāłļŗż. (
Fig. 4h) Al ļ░Å V ņØ┤ņś©ņØ┤ ņ╣śĒÖśļÉ£ NASICON Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņĀäĒśĢņĀüņØĖ ņåīĻ▓░ Ļ│ĄņĀĢņŚÉņä£ ļ│┤ļŗż SPS Ļ│ĄņĀĢņŚÉņä£ ļŹöņÜ▒ ļ░ĆļÅäĻ░Ć ļåÆņØĆ ļ»ĖņäĖ ĻĄ¼ņĪ░ ļ░Å ņ”ØĻ░ĆļÉ£ ņāüļīĆ ļ░ĆļÅäļź╝ ļéśĒāĆļāłņ£╝ ļ®░, SPS ņåīĻ▓░ ņś©ļÅäļź╝ 1000 ņŚÉņä£ 1100 ŌäāļĪ£ ļ│ĆĻ▓ĮĒĢśņŚ¼ Ļ│Āļ░ĆļÅäņØś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņ×æĒĢĀ ņłś ņ׳ņŚłļŗż. (
Fig. 4g) ļśÉĒĢ£, ņĀäĒśĢņĀüņØĖ Ļ│ĄņĀĢņ£╝ļĪ£ ņåīĻ▓░ļÉ£ LATPVļź╝ ņĀ£ņÖĖĒĢśĻ│Ā ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņŚÉņä£ļŖö ņ×ģĻ│ä ņä▒ņןņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢä ĻĘĖ Ļ▓░Ļ│╝ AlĻ│╝ VņØ┤ ļÅäĒĢæņŚÉņä£ SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņĀ£ņ×æļÉ£ LATPVļŖö ņāüņś©ņŚÉņä£ 2.6 ├Ś 10
ŌłÆ4 S cm
ŌłÆ1ņØś Ļ░Ćņן ļåÆņØĆ ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļāłĻ│Ā, 0.29 eVņØś ļé«ņØĆ ĒÖ£ņä▒ĒÖö ņŚÉļäłņ¦Ćļź╝ ļ│┤ņśĆļŗż. (
Fig. 4h) ņØ┤ ņŚ░ĻĄ¼ļŖö SPS Ļ│ĄņĀĢņØ┤ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ļ»ĖņäĖ ĻĄ¼ņĪ░ņØś ņ╣śļ░ĆĒÖöļź╝ ĒåĄĒĢ┤ ņØ┤ļĪĀ ļ░ĆļÅä(95ŌĆō97%) Ļ╣īņ¦Ć Ē¢źņāü ņØ┤ņś© ņĀäļÅäļÅäļź╝ ņ”ØĻ░Ćņŗ£Ēé¼ ņłś ņ׳ņØīņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż.
Fig.┬Ā4.
ņĀäĒśĢņĀüņØĖ ņåīĻ▓░ (conventional sintering (CS))Ļ│╝ SPSļĪ£ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś SEM, ņāüļīĆ ļ░ĆļÅä, ņØ┤ņś© ņĀäļÅäļÅä Ļ▓░Ļ│╝. (a) LiTi
2(PO
4)
3 (LTP), CS, (b) LTP, SPS, (c) Li
1.3 Al
0.3 Ti
1.7(PO
4)
3 (LATP), CS, (d) LATP, SPS, (e) Li
1.3 Al
0.3 Ti
1.7(PO
4)
2.9(VO
4)
0.1 (LATPV), CS, (f) LATPV, SPS, (g) Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØśņāüļīĆ ļ░ĆļÅä, (h) Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ņØ┤ņś© ņĀäļÅäļÅä.
26)
ļ╣äņŖĘĒĢ£ ņŚ░ĻĄ¼ļĪ£ Wen ĻĘĖļŻ╣ņŚÉņä£ļŖö ņØ┤ļĪĀ ļ░ĆļÅäņÖĆ Ļ▒░ņØś ļ╣äņŖĘĒĢ£ Ļ│Āļ░ĆļÅäļź╝ Ļ░Ćņ¦ĆļŖö Li
1.4 Al
0.4 Ti
1.6(PO
4)
3ļź╝ SPS Ļ│ĄņĀĢņŚÉ ĒåĄĒĢ┤ņä£ ņĀ£ņ×æĒ¢łļŗż.
27) SPSņØś ņåīĻ▓░ ņś©ļÅä(650 Ōäā)ļŖö ņĀäĒśĢņĀüņØĖ ņåīĻ▓░(CS (conventional sintering))ņś©ļÅä 850 Ōäāļ│┤ļŗż Ēø©ņö¼ ļé«ņĢśņ¦Ćļ¦ī SPSņŚÉ ņØśĒĢ┤ ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ņØ┤ņś© ņĀäļÅäļÅäļŖö ņ×ģņ×É Ēü¼ĻĖ░Ļ░Ć ļéśļģĖ ņŖżņ╝ĆņØ╝ļĪ£ Ļ░ÉņåīĒĢśņŚ¼ ļ░ĆļÅäļź╝ ņ”ØĻ░Ćņŗ£Ēé¼ ņłś ņ׳ņ¢┤ Ē¢źņāüļÉĀ ņłś ņ׳ļŗżļŖö Ļ▓āņØä ļ│┤Ļ│ĀĒ¢łļŗż. Duluard ĻĘĖļŻ╣ņØĆ Ļ│Āņł£ļÅäņØś Li
1.3 Al
0.3 Ti
1.7(PO
4)
3ļź╝ Solgel Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ĒĢ®ņä▒ Ēøä SPS ņåīĻ▓░ņØä ĒåĄĒĢ┤ņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņ×æĒ¢łļŗż. SPS Ļ│ĄņĀĢņ£╝ļĪ£ 850 Ōäā ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ 97%ņØś ņāüļīĆ ļ░ĆļÅäņÖĆ ņāüņś©ņŚÉņä£ 1.6 ├Ś 10
ŌłÆ4 S cm
ŌłÆ1ņØś ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļéśĒāĆļāłļŗż. ņØ┤ņÖĆ ļŗ¼ļ”¼ CSļĪ£ ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ņāüļīĆ ļ░ĆļÅäņÖĆ ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļåÆņØ┤ĻĖ░ ņ£äĒĢ┤ņä£ļŖö 1100 ŌäāņŚÉņä£ 1h ņåīĻ▓░ ņś©ļÅäņÖĆ ņŗ£Ļ░äņØ┤ ĒĢäņÜöĒ¢łļŗż. ļåÆņØĆ ņś©ļÅäņŚÉņä£ ņåīĻ▓░ņØĆ Ļ▓░ņĀĢļ”Į Ļ▓ĮĻ│äņŚÉņä£ ļ╣ä ļ”¼ĒŖ¼ ņØ┤ņś© ņĀäļÅäņä▒ 2ņ░©ņāüĻ│╝ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņŚÉņä£ ņāØņä▒ļÉśļŖö ļ»ĖņäĖ ĻĘĀņŚ┤ņØä ĒśĢņä▒ĒĢĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ SPSņŚÉ ņØśĒĢ┤ ļé«ņØĆ ņåīĻ▓░ ņś©ļÅäļŖö ņØ┤ļ¤░ ļ¼ĖņĀ£ļź╝ ĒĢ┤Ļ▓░ĒĢĀ ņłś ņ׳ļŖö ņןņĀÉņØ┤ ņ׳ļŗżĻ│Ā ļ│┤Ļ│ĀĒ¢łļŗż. ļśÉĒĢ£, LATP Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ┐Éļ¦ī ņĢäļŗłļØ╝, ļŗżļźĖ NASICON ĻĖ░ļ░ś Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņĀ£ņ×æļÉśņŚłļŗż. Ļ▓░ņĀĢņ×ģņØ┤ ņĀ£ņ¢┤ļÉ£ Li
1.5 Al
0.5 Ge
1.5(PO
4)
3 (LAGP) Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀäĻĄ¼ņ▓┤ Ļ▓░ņĀĢĒÖöņŚÉ ņØśĒĢ┤ ļ©╝ņĀĆ ņĀ£ņĪ░ Ēøä SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņ×æĒ¢łļŗż.
28) ĻĘĖ Ļ▓░Ļ│╝ 650 ŌäāņŚÉņä£ 2 minĻ░ä SPS Ļ│ĄņĀĢņ£╝ļĪ£ ņåīĻ▓░ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ 87% ņāüļīĆ ļ░ĆļÅäļź╝ Ļ░Ćņ¦Ćļ®░, ņāüņś©ņŚÉņä£ 1.3 ├Ś 10
ŌłÆ4 S cm
ŌłÆ1ņØś ņØ┤ņś© ņĀäļÅäļÅä ļ░Å 0.38 eV ĒÖ£ņä▒ĒÖö ņŚÉļäłņ¦Ćļź╝ ļéśĒāĆļāłļŗż. ņØ┤ļĀćĻ▓ī SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ£ ļé«ņØĆ ņś©ļÅäņŚÉņä£ ņåīĻ▓░ņØĆ LAGP Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņŚÉļÅä ņé¼ņÜ®ĒĢĀ ņłś ņ׳ļŗżļŖö ņןņĀÉņØä ņĀ£Ļ│ĄĒ¢łļŗż.
Perovskite ĒśĢ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łļĪ£ ņĢīļĀżņ¦ä Li
3x La
(2/3-x) TiO
3 (LLTO)ļŖö ņāüņś©ņŚÉņä£ 10
ŌłÆ3 S cm
ŌłÆ1ņØś ļåÆņØĆ ļ▓īĒü¼ ņØ┤ņś© ņĀäļÅäļÅä ļéśĒāĆļé┤ĻĖ░ ļĢīļ¼ĖņŚÉ ņĀäĻ│Āņāü ņĀäņ¦ĆņŚÉņä£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łļĪ£ ņé¼ņÜ®ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ļ¦ÄņØĆ Ļ┤Ćņŗ¼ņØä ļ░øĻ│Ā ņ׳ļŗż. ĻĘĖļ¤¼ļéś ņĀäĒśĢņĀüņØĖ ņåīĻ▓░ņØä ĒåĄĒĢ┤ Ļ│Āņł£ļÅä LLTO ņāüĻ│╝ Ļ│Āļ░ĆļÅä Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņ¢╗ĻĖ░ ņ£äĒĢ┤ņä£ļŖö ĻĖ┤ ņåīĻ▓░ ņŗ£Ļ░äĻ│╝ ļåÆņØĆ ņåīĻ▓░ ņś©ļÅä(1300 Ōäā)ļź╝ ĒĢäņÜöļĪ£ ĒĢ£ļŗż. Mei ĻĘĖļŻ╣ņØĆ 1050 ŌäāņŚÉņä£ 3 min ļÅÖņĢł SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņāüļīĆ ļ░ĆļÅä 98.5%ļź╝ Ļ░Ćņ¦ĆļŖö LLTO Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĀ£ņ×æĒ¢łņ£╝ļ®░, SPS ņåīĻ▓░ ņś©ļÅäĻ░Ć ņ”ØĻ░ĆĒĢ©ņŚÉ ļö░ļØ╝ ņāüļīĆ ļ░ĆļÅä ļ░Å ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć Ē¢źņāüļÉśļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż.
29) ĻĘĖļ¤¼ļéś SPSņŚÉ ņØśĒĢ┤ ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ļåÆņØĆ ļ▓īĒü¼ ņØ┤ņś© ņĀäļÅäļÅäļŖö 10
ŌłÆ3 S cm
ŌłÆ1ņØä ļéśĒāĆļéĖ ļ░śļ®┤ņŚÉ Ļ▓░ņĀĢ ņ×ģĻ│ä(grain boundary)ļź╝ ĒżĒĢ©ĒĢ£ ņĀäņ▓┤ņĀüņØĖ ņØ┤ņś© ņĀäļÅäļÅäļŖö 5.8 ├Ś 10
ŌłÆ6 S cm
ŌłÆ1ņØä ļéśĒāĆļāłļŗż. ņØ┤ Ļ▓░Ļ│╝ļŖö ņĀäņ▓┤ņĀüņØĖ ņØ┤ņś© ņĀäļÅäļÅäņŚÉņä£ Ļ▓░ņĀĢ ņ×ģĻ│ä(grain boundary)ņŚÉņä£ ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć ļé«ņĢä Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć Ļ░ÉņåīĒ¢łņ£╝ļ®░, Li ņåÉņŗżĻ│╝ ņ×æņØĆ ņ×ģĻ│äņŚÉņä£ La
2 Ti
2 O
5ņØś ļČłņł£ļ¼╝ ņāü ĒśĢņä▒ņ£╝ļĪ£ ņØĖĒĢ┤ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäļź╝ ļ░®ĒĢ┤ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć Ļ░ÉņåīĒĢ£ Ļ▓āņØ┤ļØ╝ ļ│┤Ļ│ĀĒ¢łļŗż. ļśÉļŗżļźĖ ņŚ░ĻĄ¼ļĪ£ LLTO Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ 1100 ŌäāņŚÉņä£ 5 min ļÅÖņĢł SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņĀ£ņ×æļÉśņŚłļŗż.
30) ņØ┤ļĀćĻ▓ī ņĀ£ņ×æļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ Ļ▓░ņĀĢ ņ×ģĻ│äņÖĆ ļ▓īĒü¼ ņØ┤ņś© ņĀäļÅäļÅä ĻĖ░ņŚ¼ņŚÉ ļīĆĒĢ┤ņä£ ņ×ÉņäĖĒĢ£ ņ¢ĖĻĖēņØĆ ņŚåņŚłņ¦Ćļ¦ī, ņĀäĒśĢņĀüņ£╝ļĪ£ LLTOĻ░Ć Ļ░Ćņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅä(10
ŌłÆ3 S cm
ŌłÆ1)ļź╝ ņāüņś©ņŚÉņä£ ļéśĒāĆļāłņ£╝ļ®░, 30.1 kj mol
ŌłÆ1ņØś ĒÖ£ņä▒ĒÖö ņŚÉļäłņ¦Ćļź╝ Ļ░Ćņ¦äļŗżĻ│Ā ļ│┤Ļ│ĀĒ¢łļŗż.
2.2 ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļź╝ ņ£äĒĢ£ SPS
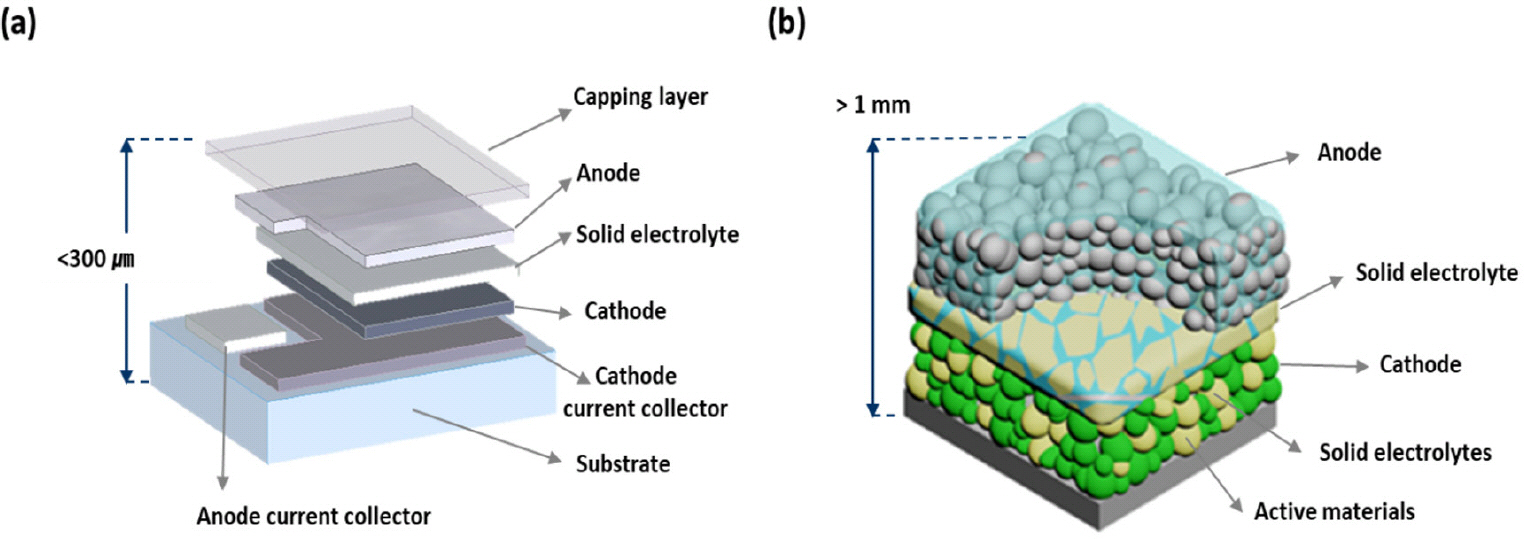
Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ņĀ£ņĪ░ ņÖĖņŚÉļÅä, SPSļŖö ņĪ░ļ░ĆĒĢśĻ│Ā ļ»ĖņäĖĒĢ£ ļ»ĖņäĖ ĻĄ¼ņĪ░ļź╝ Ļ░¢ļŖö ļ¼╝ņ¦łņØä ņĀ£ņĪ░ĒĢśļŖöļŹ░ ņ׳ņ¢┤ ņןņĀÉņØ┤ ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļź╝ ņĀ£ņĪ░ĒĢśļŖöļŹ░ ņé¼ņÜ®ļÉśņ¢┤ņÖöļŗż. ņĀäĻ│Āņāü ņĀäņ¦ĆņØś ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļŖö
Fig. 1bņŚÉņä£ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ░Å Ēāäņåī ņ▓©Ļ░Ćļ¼╝ļĪ£ ĻĄ¼ņä▒ļÉ£ļŗż. ļö░ļØ╝ņä£ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņŚÉņä£ Li ņØ┤ņś© ļ░Å ņĀäņ×ÉņØś ļ╣ĀļźĖ ņØ┤ļÅÖņØä ņ£äĒĢ┤ņä£ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ ļé┤ņŚÉ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ░Å Ēāäņåī ņ▓©Ļ░Ćļ¼╝ņØś ņĀæņ┤ēņØ┤ ņżæņÜöĒĢ£ ņŚŁĒĢĀņØä ĒĢ£ļŗż. ņØ┤Ļ▓āņØĆ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ░Å Ēāäņåī ņ▓©Ļ░ĆņĀ£ Ļ░äņØś ņÜ░ņłśĒĢ£ Ēæ£ļ®┤ ņĀæņ┤ēņØĆ Li ņØ┤ņś© ļ░Å ņĀäņ×ÉņØś ņØ┤ļÅÖļÅäļź╝ Ē¢źņāü ņŗ£ĒéżĻ│Ā, ņĀäĻĘ╣ ļ░Å ņĀäĒĢ┤ņ¦łņØś ņØæņ¦æļĀźņØä Ē¢źņāü ņŗ£ņ╝£ ņĀäĻ│Āņāü ņĀäņ¦ĆĻ░Ć Ļ░Ćņ¦ĆļŖö Ļ│äļ®┤ ņĀĆĒĢŁņØä Ļ░Éņåīņŗ£ĒéżļŖöļŹ░ ĒĢäņłśņĀüņØ┤ļŗż. ļśÉĒĢ£, ļåÆņØĆ ņČ®/ļ░®ņĀäņ£©ņØä ņ¢╗ĻĖ░ ņ£äĒĢ┤ņä£ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦łņŚÉņä£ Li ņØ┤ņś© ļ░Å ņĀäņ×ÉņØś ĒÖĢņé░ ĻĖĖņØ┤ļź╝ ņżäņØ┤ĻĖ░ ņ£äĒĢ┤ņä£ ņĀäĻ│Āņāü ņĀäņ¦ĆņŚÉņä£ ļéśļģĖ ĻĄ¼ņĪ░ ļ¼╝ņ¦łņØä ņé¼ņÜ®ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗż. ļö░ļØ╝ņä£, ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļź╝ ņäżĻ│äĒĢĀ ļĢī ņżæņÜöĒĢ£ Ļ│╝ņĀ£ļŖö ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ░Å Ēāäņåī ņ▓©Ļ░Ćļ¼╝ Ļ░äņØś ņ╣£ļ░ĆĒĢ£ ņĀæņ┤ēņØä ņŗżĒśäĒĢśļŖö ļ░®ļ▓ĢņØ┤ļ®░ ĻĄ¼ņĪ░ ļé┤ ļ»ĖņäĖĒĢ£ ņ×ģņ×É Ēü¼ĻĖ░ ļ░Å ļČäĒżļź╝ ņ£Āņ¦ĆĒĢśļŖö Ļ▓āņØ┤ļŗż.
Bouchet ĻĘĖļŻ╣ņØĆ SPS Ļ│Ąļ▓ĢņØä ņé¼ņÜ®ĒĢśņŚ¼ Li
3 V
2(PO
4)
3/ Li
3 Al
0.5 Ge
0.5(PO
4)
3/Li
3 V
2 (PO
4)
3 (LVP/LAGP/LVP)ņÖĆ LiFePO
4/Li
1.5 Al
0.5 Ge
1.5(PO
4)
3/Li
3 V
2(PO
4)
3(LFP/ LAG/ LVP)ņØś ņģĆ ĻĄ¼ņä▒ņØä Ļ░¢ļŖö ņĀäĻ│Āņāü ņĀäņ¦Ćļź╝ ņĀ£ņĪ░ĒĢśļŖö ļæÉĻ░Ćņ¦Ć ņä▒Ļ│ĄņĀüņØĖ ņé¼ļĪĆļź╝ ļ│┤Ļ│ĀĒ¢łļŗż.
31ŌĆō32)
LVP/LAGP/LVP ĻĄ¼ņä▒ņŚÉņä£ Li
3 V
2(PO
4)
3 ņĀäĻĘ╣ ļ¼╝ņ¦łņØĆ ņ×æļÅÖ ņĀäņĢĢņØ┤ 3ņŚÉņä£ 4.2 V ņé¼ņØ┤ņŚÉņä£ļŖö 120 mAh g
ŌłÆ1ņÖĆ 1.8ņŚÉņä£ 3V ņé¼ņØ┤ņŚÉļŖö 80 mAh g
ŌłÆ1ņØä ļ│┤ņŚ¼ņŻ╝Ļ│Ā, LVPņØś ņ×æļÅÖ ņĀäņĢĢņØĆ LAGPņØś ņĀäĻĖ░ ĒÖöĒĢÖņĀü ņĢłņĀĢ ņĀäņ£äĻ░Ć ņ£Āņé¼ĒĢ©ņØä Ļ░Ćņ¦Ć ĻĖ░ ļĢīļ¼ĖņŚÉ ņĀäĻ│Āņāü ņĀäņ¦Ć ļæÉ ņĀäĻĘ╣ņ£╝ļĪ£ ņäĀĒāØļÉśņŚłļŗż. (
Fig. 5a-a and 5a-b) ļæÉ ņĀäĻĘ╣ņŚÉ ļīĆĒĢ£ ņĄ£ņĀüĒÖöļÉ£ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł/Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł/Ēāäņåī ņ▓©Ļ░Ćļ¼╝ņØś ņżæļ¤ēļ╣äļŖö 25/60/15ņśĆņ£╝ļ®░, ņĀäĻĖ░ĒÖöĒĢÖ ĒģīņŖżĒŖĖļŖö ņāüņś©ņŚÉņä£ ņĢĪņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņé¼ņÜ®ĒĢśļŖö LVP/LVP ņģĆņŚÉņä£ Ļ░Ćņ¦ĆļŖö ņÜ®ļ¤ēĻ│╝ ļ╣äņŖĘĒĢ£ 80 mAh g
ŌłÆ1ņØś Ļ░ĆņŚŁņÜ®ļ¤ēņØä 80 ŌäāņŚÉņä£ ļéśĒāĆļāłļŗż. (
Fig. 5a-c and 5a-d) ņØ┤ļ▓ł ņŚ░ĻĄ¼ņŚÉņä£ 80 ŌäāņØś ņ×æļÅÖ ņś©ļÅäļŖö ņģĆņŚÉņä£ LAGPĻ░Ć Ļ░Ć ņ¦ĆļŖö ņØ┤ņś© ņĀäļÅäļÅäĻ░Ć ņĀäĻ│Āņāü ņĀäĻĖ░ ņ×æļÅÖņØä ņ£äĒĢ┤ ņÜöĻĄ¼ļÉśļŖö 10
ŌłÆ4 S cm
ŌłÆ1ņØä ĒĢäņÜöļĪ£ Ē¢łĻĖ░ ļĢīļ¼ĖņŚÉ ņäżņĀĢĒ¢łņ£╝ļ®░, SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņĀäĻ│Āņāü ņĀäņ¦Ćļź╝ ņøÉņŖżĒģØņ£╝ļĪ£ ņĀ£ņĪ░ĒĢĀ ņłś ņ׳ļŖö Ļ░ĆļŖźņä▒Ļ│╝ ņĀäņ×É ļ░Å ņØ┤ņś© ņØ┤ļÅÖņä▒ņŚÉ ļīĆĒĢ£ ĒĢ£Ļ│äņŚÉļÅä ņĀäĻ│Āņāü ņĀäņ¦ĆņŚÉņä£ ņé¼ņØ┤Ēü┤ ņÜ┤ņĀäņØ┤ Ļ░ĆļŖźĒĢśļŗżļŖö Ļ▓āņØä ļ│┤ņŚ¼ņż¼ļŗż.
Fig.┬Ā5.
(a) ņĀäĻ│Āņāü ņĀäņ¦Ć ļ¬©ņŗØļÅä ļ░Å cross-section SEM, (a)-c) LVP/LAGP/LVP ņģĆņØś ņĀäĻĖ░ĒÖöĒĢÖ ĒŖ╣ņä▒, (a)-d) LVP/LVP ņģĆņØś ņĢĪņ▓┤ ņĀäĒĢ┤ņ¦ł ņāüņŚÉņä£ ņĀäĻĖ░ĒÖöĒĢÖ ĒŖ╣ņä▒, (b)-a) ņĀäĻĖ░ĒÖöĒĢÖ ļ░śņØæ ņé¼ņØ┤Ēü┤ Ēøä LFP/LAGP/C ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņØś EIS ĒŖ╣ņä▒, (b)-b) LFP/LAGP/C ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņØś TEM Ļ▓░Ļ│╝, (b)-c) and -d) (b)-b)ņŚÉņä£ Zone 1Ļ│╝ 2ņŚÉņä£ HR-TEM Ļ▓░Ļ│╝.
31ŌĆō32)
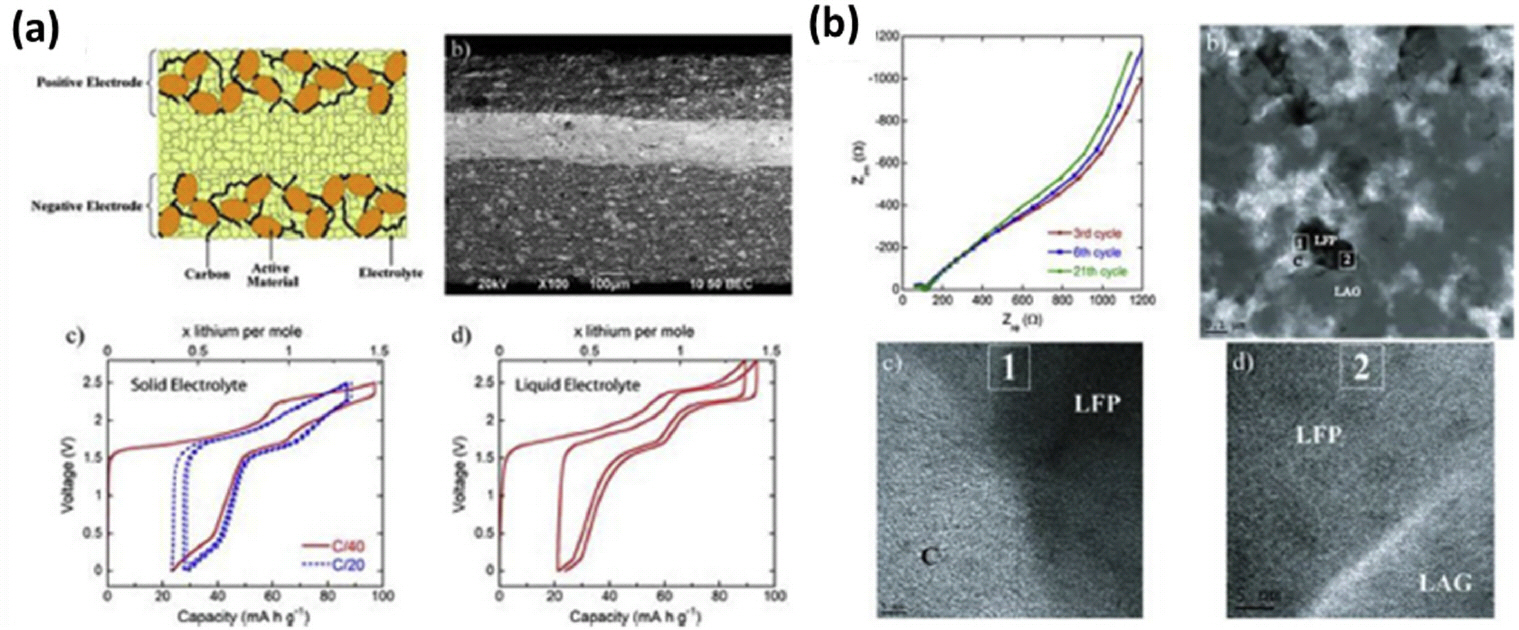
LVP/LAGP/LVP ņģĆ Ļ▓ĮņÜ░ņŚÉļŖö LFP/LVP ņżæļ¤ēļ╣äļź╝ ļæÉ ņĀäĻĘ╣ņØś ņĄ£ļīĆ Ļ░ĆņŚŁņÜ®ļ¤ēņØä ņ¢╗ĻĖ░ ņ£äĒĢ┤ņä£ 0.7ļĪ£ ņäżņĀĢĒĢśņśĆļŗż.
ņĀäĻĖ░ĒÖöĒĢÖ ĒÅēĻ░Ć Ļ▓░Ļ│╝ LVP/LAGP/LVP ņģĆņØĆ 120 ŌäāņØĖ C/20ņŚÉņä£ 80 mAh g
ŌłÆ1ņØś ņÜ®ļ¤ēņØä Ļ░Ćņ¦Ćļ®░, 30 ņé¼ņØ┤Ēü┤ ĒøäņŚÉ ņ┤łĻĖ░ ņÜ®ļ¤ēņØś 80%Ļ░Ć ņ£Āņ¦ĆļÉśļŖö ņÜ░ņłśĒĢ£ ņé¼ņØ┤Ēü┤ ĒŖ╣ņä▒ņØä ļ│┤ņśĆļŗż. ļśÉĒĢ£, ņé¼ņØ┤Ēü┤ ĒŖ╣ņä▒ Ēøä EIS ļČäņäØ Ļ▓░Ļ│╝ ņģĆ ņĀĆĒĢŁņŚÉ Ēü░ ļ│ĆĒÖöĻ░Ć ņŚåļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. (
Fig. 5b-a) ņØ┤Ļ▓░Ļ│╝ļŖö ņé¼ņØ┤Ēü┤ ĒøäņŚÉ TEM ļČäņäØņØä ņé¼ņÜ®ĒĢśņŚ¼ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łĻ│╝ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł Ļ░äņØś ņØĖĒä░ĒÄśņØ┤ņŖżļź╝ ļČäņäØĒĢ£ Ļ▓░Ļ│╝ ņĀäĻĘ╣ņŚÉņä£ ĻĘĀņŚ┤ņØ┤ ļ░£ņāØļÉśņ¦Ć ņĢŖĻ│Ā, LFP, Ēāäņåī ņ▓©Ļ░ĆņĀ£ ļ░Å Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł Ļ░äņØś ņÜ░ņłśĒĢ£ ņĀæņ┤ēņØä ņ£Āņ¦ĆĒĢśĻ│Ā ņ׳ņ¢┤ ņģĆņØ┤ Ļ░Ćņ¦ĆļŖö ņä▒ļŖźņØä ņ£Āņ¦ĆĒĢĀ ņłś ņ׳ļŖö Ļ▓āņØ┤ļØ╝ ļ│┤Ļ│ĀĒ¢łļŗż. (
Fig. 5b-c and 5b-d) ļśÉĒĢ£, ņØ┤ļ▓ł ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäĻ│Āņāü ņģĆ ļé┤ņŚÉ 15%ņØś ņ×öļźś ĻĖ░Ļ│ĄņØĆ ņĀäĻĖ░ ĒÖöĒĢÖ ļ░śņØæ Ļ│╝ņĀĢņŚÉņä£ LFPņÖĆ LVPņØś ĻĄŁļČĆ ņØæļĀźņØä ņÖäĒÖö Ļ░ĆļŖź ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņĀäĻĘ╣ņŚÉ Ļ▓░ĒĢ©ņØä ņŚåĻ▓ī ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ĒĢäņłśņĀüņØ┤ļØ╝Ļ│Ā ņĀ£ņĢłĒ¢łļŗż. ņל ņĢīļĀżņ¦ä ļ░öņÖĆ Ļ░ÖņØ┤, ļ”¼ĒŖ¼ĒÖö ļ░Å Ēāłļ”¼ĒŖ¼ (lithiation and delithiation) Ļ│╝ņĀĢ ļÅÖņĢłņŚÉ ņĀäĻĘ╣ ļ¼╝ņ¦łņØś ļČĆĒö╝ ļ│ĆĒÖöļŖö ņĀäĒĢ┤ņ¦łļĪ£ļČĆĒä░ ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦łņØś ļ░Ģļ”¼ļź╝ ņĢ╝ĻĖ░ Li ņØ┤ņś©ņØś ĒÖĢņé░ Ļ▓ĮļĪ£ļź╝ ļ░®ĒĢ┤ĒĢĀ ņłś ņ׳ņ¢┤, ņØ┤ļ▓ł ņŚ░ĻĄ¼ļŖö ņØśļÅäņĀüņ£╝ļĪ£ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņŚÉ ņ×öļźś ĻĖ░Ļ│ĄņØä ņĪ┤ņ×¼ ņŗ£Ēé┤ņ£╝ļĪ£ ņĀäĻĘ╣ Ļ▓░ĒĢ© ļ¼ĖņĀ£ņŚÉ ļīĆĒĢ£ ĒĢ┤Ļ▓░ņ▒ģņØä ņĀ£ņŗ£Ē¢łļŗż.
ņĄ£ĻĘ╝ ņŚ░ĻĄ¼ņŚÉņä£ SPSļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĀäĻ│Āņāü LiCoO2(LCO) ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļź╝ ņĀ£ņĪ░ĒĢśĻ│Ā, Li ĻĖłņåŹņØä ņāüļīĆ ņĀäĻĘ╣ņ£╝ļĪ£ ņé¼ņÜ®ĒĢśņŚ¼ ņĀäĻ│Āņāü ņĀäņ¦ĆņØś ņä▒ļŖźņØä ĒÅēĻ░ĆĒ¢łļŗż.
LeeņÖĆ ļÅÖļŻī ņŚ░ĻĄ¼ņ×ÉļōżņØĆ LCO, Li
5 La
3 Ta
2 O
12 (LLTO)ņÖĆ Ēāäņåī ļéśļģĖĒŖ£ļĖī(MWCNTs) ņé¼ņØ┤ņØś ņżæļ¤ēļ╣äļź╝ SPS Ļ│ĄņĀĢņØä ĒåĄĒĢ┤ ņĄ£ņĀüĒÖöĒĢśņŚ¼ ņĀäņ×É ļ░Å Li ņØ┤ņś© ņĀäļÅäļź╝ Ļ░Ćņ¦ĆļŖö ņĀäĻ│Āņāü ņĀäņ¦Ćļź╝ ĻĄ¼ĒśäĒ¢łļŗż.
33) ņĄ£ņĀüņØś ņĪ░ņä▒ņØĆ ņżæļ¤ēļ╣äļĪ£ 32LCO/ 65LLTO/3MWCNTsņØ┤Ļ│Ā, ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļŖö 600 ŌäāņŚÉņä£ 5 min ļÅÖņĢł SPS Ļ│ĄņĀĢņŚÉ ņØśĒĢ┤ ņåīĻ▓░ļÉśņŚłļŗż. (
Fig. 6a) ņĀäĻ│Āņāü ņĀäņ¦Ć ņĀ£ņ×æņØä ņ£äĒĢ┤ ņé¼ņÜ®ļÉ£ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņÖĆ Ļ│äļ®┤ ņĢłņĀĢņä▒ņØä ņ”ØĻ░Ć ņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ņä£ ļ╣äņĀĢņ¦łĻ│ä LIPON ņØä ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ ņ£äņŚÉ PVD Ļ│Ąļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ”Øņ░®ĒĢśņśĆļŗż. (
Fig. 6d) ņāüļīĆ ņĀäĻĘ╣ņ£╝ļĪ£ Li ĻĖłņåŹņØä ņé¼ņÜ® ņĀäĻ│Āņāü ņĀäņ¦Ćļź╝ ņĀ£ņ×æ ņĀäĻĖ░ĒÖöĒĢÖ ĒÅēĻ░Ćļź╝ ņ¦äĒ¢ēĒĢ£ Ļ▓░Ļ│╝ LCO/LLTO/ MWCNTs ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ļŖö 80 ŌäāņŚÉņä£ 0.05 CņØś ņĀäļźś ļ░ĆļÅäņŚÉņä£ 0.3 mAh cm
ŌłÆ3ņØś ļ░®ņĀä ņÜ®ļ¤ēņØä ļéśĒāĆļāłļŗż. (
Fig. 6c-a and 6c-b) ļśÉĒĢ£, 10 ņé¼ņØ┤Ēü┤ ĒøäņŚÉļÅä ņĀäĻĘ╣Ļ│╝ ņĀäĒĢ┤ņ¦ł Ļ│äļ®┤ņŚÉņä£ ņĢłņĀĢņä▒ ļ░Å ņĀäĻĖ░ĒÖöĒĢÖ ļ░śņØæņŚÉ ļö░ļźĖ ņĀäĻĘ╣ ļ¼╝ņ¦łņØ┤ ņĀäĒĢ┤ņ¦łļĪ£ ĒÖĢņé░ļÉśļŖö ņĢŖļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż. (
Fig. 6b)
Fig.┬Ā6.
(a)-a) and -b) LCO/LLTO/MWCNTs ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ ņØ┤ļ»Ėņ¦Ć, (a)-c) and -d) LiPON ļ░Ģļ¦ēĒśĢ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØ┤ ņ”Øņ░® ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņØś SEM Ļ▓░Ļ│╝, (b) ņČ®ļ░®ņĀä ņé¼ņØ┤Ēü┤ Ēøä ņĀäĻĘ╣Ļ│╝ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł Ļ│äļ®┤ņŚÉņä£ EDS Ļ▓░Ļ│╝, (c) LCO/LLTO/MWCNTs ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņØś ņČ®ļ░®ņĀä ļ░Å ņé¼ņØ┤Ēü┤ ĒŖ╣ņä▒, (d) LCO/LLTO/MWCNTs ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņÖĆ LIPON ļ░Ģļ¦ē Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł Ļ│äļ®┤ņŚÉņä£ TEM Ļ▓░Ļ│╝.
33)

ļŗżļźĖ ņŚ░ĻĄ¼ļĪ£ LCO/Li
2.2 C
0.8 B
0.2 O
3 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łĻ│╝ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ ņĀ£ņ×æĒĢśĻĖ░ ņ£äĒĢ┤ņä£ SPS Ļ│ĄņĀĢņØä ņé¼ņÜ®Ē¢łļŗż.
34) Li
2.2 C
0.8 B
0.2 O
3 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØĆ ņāüņś©ņŚÉņä£ 1 ├Ś 10
ŌłÆ6 S cm
ŌłÆ1ļź╝ Ļ░ĆņĪīņ¦Ćļ¦ī, ņĀäĻ│Āņāü ņĀäņ¦ĆļŖö 60 ŌäāņØś ņĀĢņĀäļźś 10 ╬╝A cm
ŌłÆ2ņŚÉņä£ 120 mAh g
ŌłÆ1ņØś ņ┤łĻĖ░ņÜ®ļ¤ēņØä ļéśĒāĆļāłņ£╝ļ®░, 10 ņé¼ņØ┤Ēü┤ ĒøäņŚÉ 100 mAh g
ŌłÆ1ņØä ņ£Āņ¦ĆĒ¢łļŗż. ņØ┤ļ¤░ ņÜ®ļ¤ē ņĀĆĒĢśļŖö ļ░śļ│ĄļÉśļŖö ņĀäĻĘ╣ņØś ĒīĮņ░ĮĻ│╝ ņłśņČĢņ£╝ļĪ£ ņØĖĒĢ£ ņĀäĻĘ╣Ļ│╝ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł Ļ│äļ®┤ņŚÉņä£ ņĢłņĀĢņä▒ ņĀĆĒĢśļĪ£ ņØĖĒĢ£ Ļ▓āņØ┤ļØ╝ ĒīÉļŗ©Ē¢łļŗż. SPS Ļ│ĄņĀĢņ£╝ļĪ£ ņĀ£ņĪ░ļÉ£ ņĀäĻ│Āņāü ņĀäņ¦ĆņØś ņÜ░ņłśĒĢ£ ņĀäĻĖ░ ĒÖöĒĢÖņĀü ņä▒ļŖźņØĆ Li
2.2 C
0.8 B
0.2 O
3 Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łĻ│╝ LCO Ļ│äļ®┤ņŚÉņä£ ņĀæņ┤ē ņĀĆĒĢŁņØ┤ ļé«ĻĖ░ ļĢīļ¼ĖņŚÉ ņ¢╗ņ¢┤ņ¦ä Ļ▓āņØ┤ļ®░, ņØ┤ļ▓ł ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ┤ ņĀäĻĘ╣Ļ│╝ ņĀäĒĢ┤ņ¦ł ņé¼ņØ┤ņØś Ļ│äļ®┤ņØĆ ņĀäĻ│Āņāü ņĀäņ¦ĆĻ░Ć Ļ░Ćņ¦ĆļŖö ņä▒ļŖźņØä Ē¢źņāüņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ņä£ ņżæņÜöĒĢ£ ņÜöņåīļØ╝Ļ│Ā ņĀ£ņĢłĒ¢łļŗż.
ņĄ£ĻĘ╝ SPS Ļ│ĄņĀĢņØĆ Na
3 V
2(PO
4)
3/Na
3 Zr
2 Si
2 PO
12/ Na
3 V
2(PO
4)
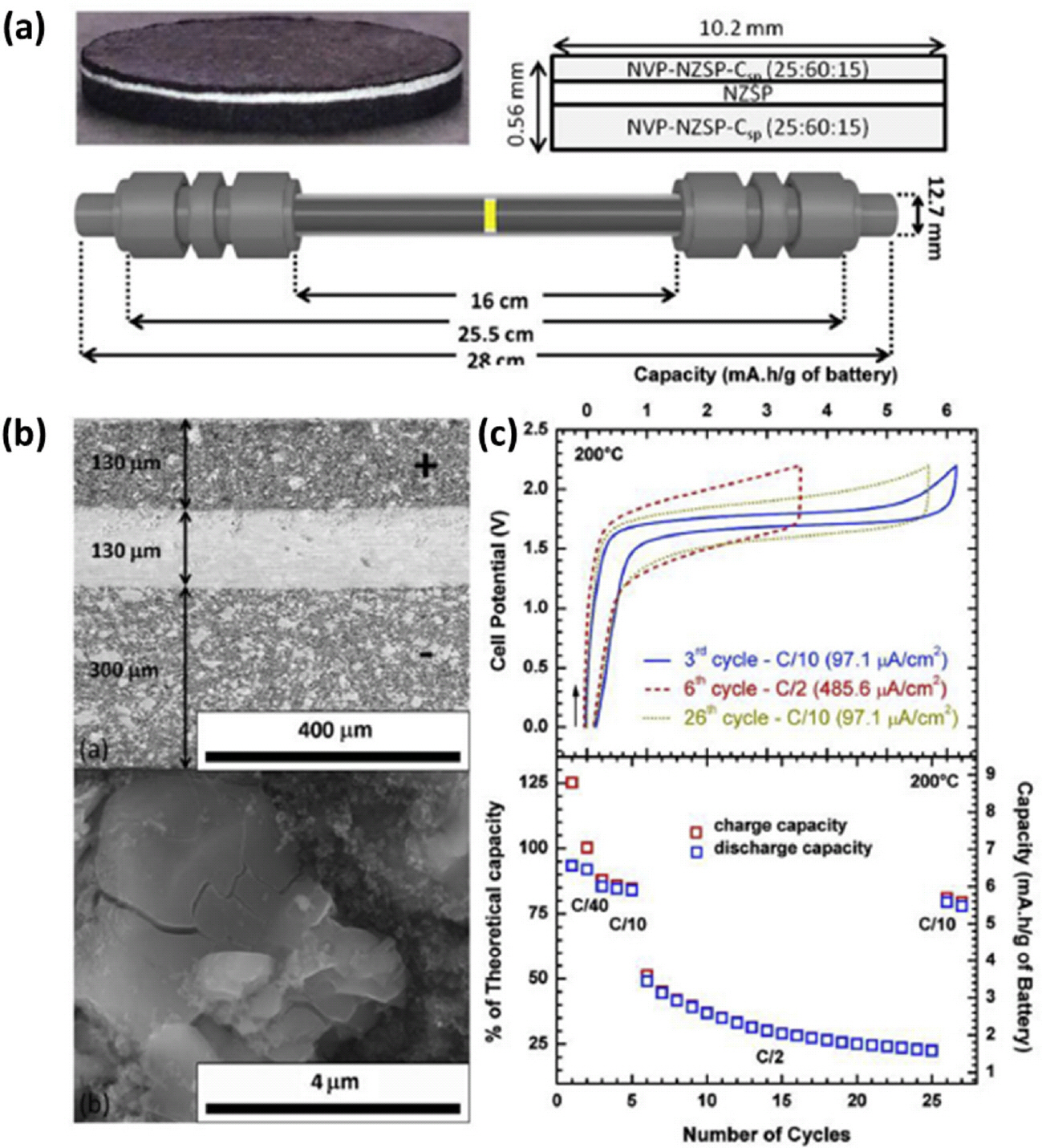
3 (NVP/NZSP/NVP) ņģĆņØä ĻĖ░ļ░śņ£╝ļĪ£ ĒĢśļŖö ņäĖļØ╝ļ»╣ Ļ│Āļ░ĆļÅä Na ņØ┤ņś© ņĀäņ¦Ć (ņ×æļÅÖ ņś©ļÅä: 200 Ōäā)ļź╝ ņĀ£ņĪ░ĒĢśļŖöļŹ░ ņ▓śņØīņ£╝ļĪ£ ņé¼ņÜ®ļÉśņŚłļŗż.
35) Na
4 V
2(PO
4)
3 (ņØīĻĘ╣ņŚÉņä£ ĻĄÉĒÖś ļÉ£ 1 Na
+)ņØĆ NaV
2(PO
4)
3 (ņ¢æĻĘ╣ņŚÉņä£ ĻĄÉĒÖś ļÉ£ Na
+)ļĪ£ ņé░ĒÖö ļÉĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ Na
3 V
2(PO
4)
3ņØĆ ļæÉ ņĀäĻĘ╣ņŚÉņä£ ļ¬©ļæÉ ņé¼ņÜ®ļÉśņŚłņ£╝ļ®░, ņĀäĻ│Āņ▓┤ NVP/NZSP/NVP ņģĆņØä ņĀ£ņĪ░ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ņĀäĻĘ╣ņŚÉ ĒżĒĢ©ĒĢśļŖö ņĀäĻĘ╣ ĒÖ£ļ¼╝ņ¦ł, Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦ł ļ░Å ņ╣┤ļ│Ė ļÅäņĀäņĀ£ņØś ĒĢ©ļ¤ēņØä 25NVP/60NZSP/15ļĪ£ ņĀäĻĘ╣ ļ│ĄĒĢ®ņ▓┤ņÖĆ Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØä ņĖĄļ│äļĪ£ ĒśĢņä▒ Ēøä SPS Ļ│ĄņĀĢņØä ņØ┤ņÜ® 900 Ōäā ņŚÉņä£ ņåīĻ▓░ņØä ĒåĄĒĢ┤ ņĀ£ņ×æĒĢśņśĆļŗż. (
Fig. 7(a)) Ļ░ü ņĀäĻĘ╣ ļé┤ņŚÉ NVPņÖĆ NZSP ņ×ģņ×ÉļŖö ļåÆņØĆ ļČäņé░ļÅäļź╝ Ļ░ĆņĪīņ£╝ļ®░, ņĀäĻ│Āņāü ņĀäņ¦Ć ļæÉ ņĀäĻĘ╣ ļ░Å Ļ│Āņ▓┤ ņĀäĒĢ┤ņ¦łņØś ļæÉĻ╗śļź╝
Fig. 7(b)ņŚÉ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņĀäĻ│Āņāü ņĀäņ¦ĆĻ░Ć Ļ░Ćņ¦ĆļŖö ņĀäĻĖ░ĒÖöĒĢÖ ĒŖ╣ņä▒ņØä Ļ░Ćņ¦Ć ņ£äĒĢ┤ņä£ ņĄ£ņĀüĒÖöĒĢ┤ ļéśĒāĆļāłļŗż. ņĀäĻ│Āņāü ņĀäņ¦ĆĻ░Ć Ļ░Ćņ¦ĆļŖö ņĀäĻĖ░ĒÖöĒĢÖ ĒŖ╣ņä▒ ĒÅēĻ░Ć Ļ▓░Ļ│╝ ņĀäĻ│Āņāü ņĀäņ¦ĆĻ░Ć Ļ░Ćņ¦ĆļŖö ļ░®ņĀä ĒŖ╣ņä▒ C/40 ņĀäļźś ļ░ĆļÅäņŚÉņä£ 6.5 mAh g
ŌłÆ1 Ļ░Ćņ¦ĆļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łļŗż.ņØ┤ļ¤░ ņÜ░ņłśĒĢ£ ņä▒ļŖźņØĆ 30 ņé¼ņØ┤Ēü┤ ņČ®/ļ░®ņĀä ĒøäņŚÉļÅä NVP, NZSPņÖĆ ņ╣┤ļ│Ė ņ▓©Ļ░ĆņĀ£ņØś ņÜ░ņłśĒĢ£ Ļ│äļ®┤ ņĢłņĀäņä▒ņ£╝ļĪ£ ņØĖĒĢ┤ ņ£Āņ¦ĆļÉ£ļŗżļŖö Ļ▓āņØä ņĀ£ņŗ£Ē¢łņ£╝ļ®░, ņØ┤ Ļ▓░Ļ│╝ļŖö ņĀäĻ│Āņāü ņĀäņ¦Ć NVP/ NZSP/NVP ņģĆņØś ņŚÉļäłņ¦Ć ļ░ĆļÅäļŖö C/10ņŚÉņä£ ņĢĮ 1.0 mAh cm
ŌłÆ2 ļĪ£ ņØ┤ļŖö ņåīņ×¼Ļ░Ć Ļ░Ćņ¦ĆļŖö ņØ┤ļĪĀ ņÜ®ļ¤ēņØś 85%ļØ╝ļŖö Ļ▓āņØä ļ│┤Ļ│ĀĒ¢łļŗż.
Fig.┬Ā7.
(a) NVP/NZSP/NVP ņģĆ ĻĄ¼ņĪ░, (b) 30 ņé¼ņØ┤Ēü┤ Ēøä ņĀäĻ│Āņāü NVP ņ×ģĻ│äĻ░Ć Ļ░Ćņ¦ĆļŖö ļ»ĖņäĖĻĄ¼ņĪ░ Ļ▓░Ļ│╝, (c) NVP/NZSP/NVP ņģĆņØ┤ Ļ░Ćņ¦ĆļŖö ņČ®/ļ░®ņĀä ĒŖ╣ņä▒ ļ░Å ņé¼ņØ┤Ēü┤ ņĢłņĀäņä▒ Ļ▓░Ļ│╝
35)